Il pacchetto di esami diagnostici per diagnosi di Chikungunya comprende:
– test sierologico per la ricerca degli anticorpi contro il virus;
– emocromo, ves, PCR, mucoproteine, elettroforesi proteica.
La diagnosi finale è elaborata dal medico anche con la valutazione di altre analisi cliniche
Per informazioni e prenotazioni di visita e test telefona al numero: 06/39030481 oppure scrivi una mail all’indirizzo [email protected]
Per le urgenze puoi contattare il Call Center Travel Health, attivo 24 ore su 24 al numero 06/43236290
SCHEDA MALATTIA
Descrizione: La Chikungunya è una malattia infettiva, virale acuta febbrile, presente nelle aree tropicali ed equatoriali, e sempre più negli ambienti tropicalizzati, degli USA, del bacino del mediterraneo, oltre che della Cina, Giappone e Filippine, e dell’Australia. E’ trasmessa attraverso la puntura di zanzare, femmine, infette, di diversi generi, presenti sia in ambiente urbano che in ambiente silvestre e selvaggio. Si manifesta con sintomi simili a quelli di altri virus, quali quelli influenzali, ma con caratteristiche precise ed inequivocabili: febbre elevata, cefalea persistente, stanchezza ingravescente e profonda, e soprattutto, una infiammazione delle articolazioni e dei muscoli con importanti dolori che talora costringono il paziente ad assumere una posizione piegata, contorta, nel tentativo di alleviare la sofferenza (nella lingua africana swahili, “chikungunya” significa “ciò che curva” o “contorce”). Il quadro è spesso accompagnato da manifestazioni cutanee maculo papulari, pruriginose, che talora possono assumere caratteristiche di tipo emorragico transitorio quali petecchie, ecchimosi, epistassi, gengivorragie. Il serbatoio è l’uomo, portatore del virus, che può essere sano, pauci sintomatico (lievi sintomi) oppure malato. E’ da chiarire bene che la trasmissione del virus non avviene per contatto diretto tra persona e persona, ma sono le zanzare, in particolari Aedes, che, attraverso la puntura, trasmettono la malattia, da uomo ad uomo.
Agente infettivo
Ciclo vitale
Porta di ingresso
Distribuzione
Incubazione
Sintomi
Controllo e prevenzione
Trattamento
Diagnosi
Agente infettivo:
l virus responsabile della “Chikungunya” appartiene alla famiglia delle “Togaviridae” (Arbovirus), del genere degli “Alphavirus”. Tra questi virus importanti West Nile Virus, l’encefalite equina dell’Est, altri virus neurotropi, i cui serbatoi sono sia uccelli che animali, ed in particolare equinidi. Virus simili sono l’ O’nyong-nyong virus ed il Sindbis virus.
Ciclo vitale:
Diverse sono le specie di zanzare coinvolte nella trasmissione nella diffusione e nel mantenimento del virus chikungunya (CHIKV) in natura. I vettori specifici sono la Aedes, Aegypti e Polynesiensis, nelle epidemie urbane con principale serbatoio umano. La Aedes Albopictus, conosciuta in Europa come ‘zanzara tigre’, presente in Oriente, ma anche nelle aree temperate del vecchio continente e degli USA, mantiene i livelli di trasmissione. La zanzara Culex, presente nel bacino del mediterraneo, ha dimostrato capacità di infettarsi e trasmettere il virus. In Africa, in particolare nelle savane e nelle aree silvestri, Aedes Africanus ed artropodi del genere Mansonia sono responsabili della trasmissione. In ambiente rurale e delle savane i serbatoi prevalenti sono costituiti da scimmie (babbuini) e circopitechi, oltre che altri piccoli mammiferi e roditori. Per questo motivo la malattia si mantiene e si diffonde.
La trasmissione verticale (da zanzara madre alla larvac/ figlia) del virus Chikungunja è presente e dimostrata in Aedes Aegypti, Africanus ed altri…, anche per altri virus quali dengue o Zika, e questo è uno dei motivi del mantenimento della trasmissione della malattia nei territori coinvolti. Ma la trasmissione verticale non è stata dimostrata in Aedes Albopictus, nel bacino del mediterraneo, e questo costituirebbe un altro motivo di difficoltà di attecchimento del virus nei territori europei. Quindi la competenza vettoriale di Aedes Albopictus è fortemente ridotta e l’efficacia di trasmissione difficoltosa, fino ad oggi.
La vita della zanzara della CHIKV è stimata tra 15 e 30 giorni. Il tempo di replicazione del virus nelle ghiandole salivari della zanzara è di circa 10 giorni. Questi dati confermano la possibilità dello sviluppo di una popolazione di zanzare infette in un ambiente favorevole. Inoltre bisogna tener presente che le uova di Aedes Albopictus possono sopravvivere disseccate per molti mesi, anche in ambienti secchi e freddi. Una volta inoculato il virus dalla zanzara all’uomo, e passata la barriera cutanea e dermica indenne, la viremia, la presenza del virus nel sangue, dura tra i 3 ed i 10 giorni, periodo immediatamente precedente l’inizio dei sintomi, fino al 5 giorno in cui il paziente è sintomatico. Durante questo periodo la zanzara ha possibilità di contagiarsi ed innescare nuovamente il processo.
Porta d’ingresso:
Gli Alphavirus e tra questi diversi Togavirus (chikungunya) sono diffusi in tutto il mondo tropicale, equatoriale ed anche, per il surriscaldamento del pianeta, come era stato previsto da decenni, in molte parti dei paesi temperati, sempre più caldi. Sono considerate antropo zoonosi, presenti in diversi animali, in grado di causare malattie anche all’uomo. La causa dei contagi e quindi delle infezioni da Alfavirus sono alcuni artropodi, che diventano vettori, vettori, soprattutto zanzare del genere Aedes, ma anche Culex. Anopheles non può contagiarsi con questo microrganismo. il virus non si trasmette da persona a persona con i normali contatti di vita quotidiana, né per via aerea o rapporto sessuale. Comunque non si può escludere in modo assoluto la possibilità di un contagio interumano (per via aerea, per contatto con fluidi organici…) specialmente tra soggetti che restano in prolungato contatto con malati. Possibile ma difficile la trasmissione attraverso le trasfusioni.
Modalità di infezione:
Gli artropodi, ed in particolare le zanzare, si contagiano con i virus cibandosi ed ingerendo, piccolissime quantità di sangue infettato dal virus. Durante la viremia, presenza di virus nel sangue, in soggetti sani o malati, i virus ingeriti, si moltiplicano nei tessuti della zanzara, ed in particolare nelle “ghiandole salivari”. Occorre sottolineare, per motivo epidemiologico, che nella maggior parte dei casi gli animali, ma anche l’uomo appaiono sani e non malati, anche leggermente. Molti gli esempi di portatori di virus (SERBATOIO) sia negli uccelli, che nei mammiferi. Si ribadisce che l’uomo, portatore sano, che non manifesta i sintomi, può infettare una zanzara che punge, in fase di viremia.
Una volta che un vertebrato, uccello o mammifero, viene morso da una zanzara infetta, questa attraverso la sua saliva, inietta il virus, nel derma e da qui, attraverso le cellule endoteliali dei capillari, nel flusso sanguigno, causando la “viremia” (presenza del virus nel sangue). In questa prima fase le difese naturali della cute e del derma, con i loro sistemi immuni e le reazioni infiammatorie, possono neutralizzare, come avviene nella maggior parte degli individui punti, il virus inoculato, ed il contagio e l’infezione non avviene. In questo caso possono essere rilevati movimenti immunitari tramite diagnostica sierologica. (ma l’infezione non è avvenuta).
Questa è una delle motivazioni per cui il virus, presente sporadicamente (in pochi individui portatori del microrganismo), difficilmente può attecchire in altri individui presenti nel territorio in modo stabile (autoctoni) e che non hanno mai avuto il contatto con il virus. Per innescare un focolaio epidemico e diffondere la malattia, occorre la presenza di molti serbatoi (individui o animali) infetti e di zanzare che ripetutamente pungono il serbatoio. Evento veramente eccezionale. E’ più verosimile che si presentino casi di malattia sporadica che non l’innesco di un fenomeno che si eradica sul territorio.
Talvolta quindi compare la malattia, che si manifesta ad episodi singoli nei territori dove la malattia non esiste. Nel singolo individuo la comparsa delle malattie da Alphaviridae, e tra queste Chikungunia, trova nel sistema immunitario di superficie ( cutaneo – dermico) ed in quello profondo, un sistema di sicurezza importante. Nell’immunità specifica, indotta dai virus sono coinvolti Linfociti di tipo T, cellule di tipo B con formazione di anticorpi neutralizzanti. Vengono innescati i processi infiammatori di protezione tissutale, e si attiva anche la produzione di interferone.
Distribuzione:
Il virus della “Chikungunya” è stato descritto la prima volta nel 1952 in Tanzania, nelle savane al confine con il Kenia ed in diversi villaggi sulle coste del lago Vittoria e nell’entroterra. Le prime segnalazione cliniche di febbri “spaccaossa” risalgono al 1779, in Indonesia dove venne descritta un’epidemia di febbri dolorose forse attribuibile allo stesso agente virale. Dagli anni ‘50 diverse epidemie di chikungunya si sono verificate in Asia ed Africa. A partire dal 2005, sono stati riportati ampi focolai nell’area dell’Oceano Indiano (India, Malaysia, La Reunion, Madagascar, Indonesia, Mauritius, Mayotte, Seychelles). In tutte queste aree, comprese le isole dell’Oceano Indiano, il virus trova il suo habitat ideale. In molte aree orientali africane e da qualche anno in molti paesi dell’America Latina, questa malattia coesiste con la dengue ed i sintomi delle due malattie si sovrappongono. Molto spesso non è facile fare la diagnosi differenziale fra le due malattie. L’incidenza di “chikungunya” è sicuramente sottostimata sia per i casi lievi e paucisintomatici che si presentano e non vengono diagnosticati, sia per la diffusione mediante l’alta percentuale di portatori sani del virus. Nei paesi dell’area tropicale ed equatoriale la diagnosi è prevalentemente clinica e non di laboratorio per mancanza dei kit. Nei sistemi sanitari di questi paesi è quasi impossibile la conferma con test di laboratorio, e difficilmente viene eseguita la diagnosi clinica. Per i tropicalisti che lavorano e conoscono i sistemi clinici è facile capire come, in questi paesi, tutte le malattie vengono classificate come malaria e tifo. Le altre ipotesi di patologie, soprattutto virali, non vengono prese in considerazione. Dove il virus circola, durante le epidemie, il virus può infettare da un terzo a quattro quinti dell’intera popolazione, con drammatiche conseguenze sullo stato fisico di interi cluster di abitanti. A fine 2013 la prima epidemia di Chikungunja, riportata in America Latina, in alcune isole Caraibiche. Dalla fine del 2014 oltre un milione di casi sono stati riportati in diversi paesi Caraibici, dell’America Centrale e del Sud. Il virus continua a circolare e sono spesso coinvolti anche viaggiatori che provengono da aree temperate.
Commenti sui casi di Chikungunya nel Lazio (Settembre 2017)
Casi di Chikungunya nel mondo al 29 Maggio 2018. Sono esclusi i paesi che hanno registrato solo casi importati.
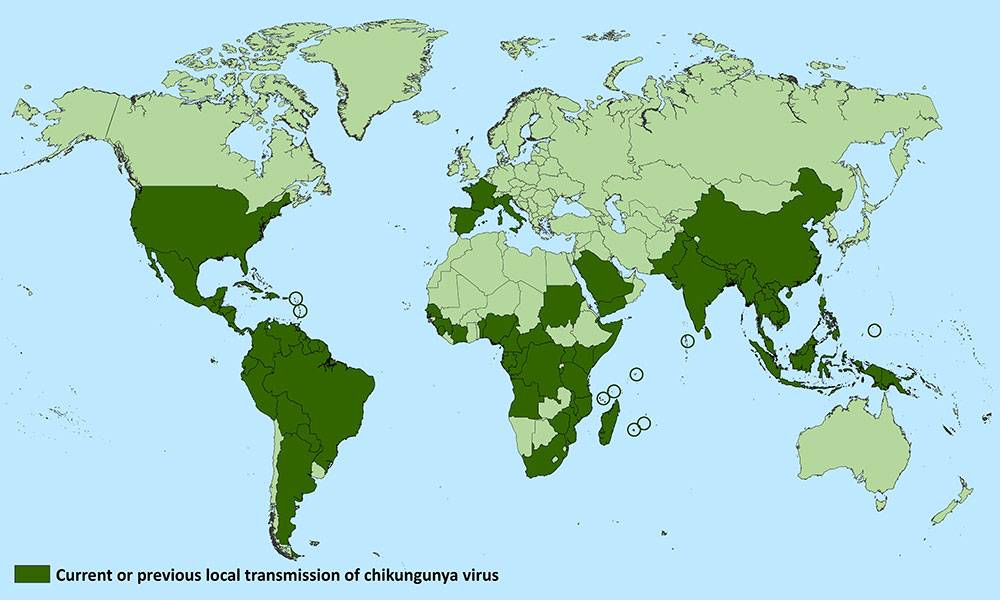
CDC- YELLOW BOOK, 2018 – Paesi in cui è diffuso il rischio di malattie trasmesse da zanzare del genere Aedes.
A partire da marzo del 2005, a La Rèunion e in altre zone dell’Oceano Indiano è scoppiata un’importante epidemia di chikungunya. A distanza di un anno (17 marzo 2006), l’Organizzazione mondiale della sanità ha stimato circa 204.000 persone infettate a La Rèunion, pari a circa un terzo della popolazione totale (705.000 abitanti). In India, tra febbraio e ottobre 2006, l’epidemia di chikungunya ha coinvolto 8 stati o province: i casi sospetti arrivano fino a 1,25 milioni. Dal 2013 al 2016 i casi si sono moltiplicati e diffusi a macchia d’olio. Si calcola che diverse centinaia di milioni di individui siano stati affetti dal virus e mantengano la presenza di virus nel sangue.
In Europa prevalentemente la zanzara tigre (Aedes Albopictus), vettore dell’infezione, è ampiamente diffusa in particolare nelle aree rivierasche del mediterraneo. Il numero di casi segnalati in Europa al 13 giugno 2006 è stato rispettivamente di: 307 casi in Francia, 17 casi in Germania, 12 casi in Belgio, 9 casi nel regno Unito, 1 caso in Norvegia, 1 caso nella Repubblica Ceca. In Italia sono stati confermati, alla stessa data, 11 casi in pazienti che avevano viaggiato in paesi endemici. Oltre a questi pazienti, che avevano acquisito l’infezione all’estero, in Francia è stato segnalato un probabile caso autoctono. Si trattava di un infermiere che aveva assistito un paziente con chikungunya, acquisendo probabilmente l’infezione attraverso esposizione accidentale al sangue, durante la fase viremica.
In Europa, la possibilità di trasmettere l’infezione da parte della zanzare tigre, dipende da caratteristiche climatiche, di densità di popolazione suscettibile e densità dei flussi migratori, data da persone asintomatiche o sintomatiche che hanno contratto la malattia in altri luoghi. Importanti aspetti da analizzare sono costituiti dallo stato d’interazione ospite/vettore, dati dallo stato immunitario dell’ospite, dalla concentrazione di virus nel sangue dell’ospite, da precedenti infezioni da ceppi virali diversi. In molti Paesi europei (Francia, Germania, Norvegia, Svizzera) la febbre chikungunya è stata diagnosticata a viaggiatori provenienti da aree epidemiche, ma la trasmissione in loco da parte delle zanzare non era mai stata riportata. Il rischio, al momento attuale, è comunque considerato limitato a piccole aree, soprattutto nelle nazioni dell’Europa meridionale, tra cui l’Italia, ossia l’Europa mediterranea.
In Italia nella seconda metà di agosto 2007, la regione Emilia Romagna ha notificato un focolaio epidemico di casi d’infezione virale, trasmessa da insetti, nella provincia di Ravenna. E’ stato poi tempestivamente confermato che i casi sono stati causati da infezione da virus Chikungunya. I casi riportati al 4 settembre 2007 sono in totale 197. Di questi, 166 rientrano completamente nei criteri di definizione di caso: 147 provengono dal focolaio iniziale che si è verificato nell’area di Castiglione di Cervia e Castiglione di Ravenna, due piccole cittadine separate da un fiume, mentre 19 da cluster secondari nelle periferie di Cesena (13 casi) e Cervia (6 casi). Sul fronte dei casi confermati di laboratorio, al 14 settembre risultano 101 casi positivi, 33 negativi e 133 in attesa di esito. 2 casi di malattia sono stati inoltre segnalati, tempestivamente, dalla Regione Lombardia, in soggetti che avevano soggiornato nelle suddette aree. Inoltre, il virus chikungunya è stato ritrovato nella zanzara Aedes albopictus.
Nell’Agosto 2017 sono stati segnalati e denunciati tre casi accertati di Chikungunja nel comune di Anzio, in provincia di Roma. Sono state trovate alcune zanzare infette, ed i focolai sono stati immediatamente bonificati. Il focolaio sembra essere costituito da casi sporadici.
Incubazione:
Il periodo di incubazione da vai 3 ai 10 giorni, in media 4-6 giorni. La malattia ha un andamento tipicamente bifasico.
Sintomi:
Nella prima fase della malattia manifesta, che dura dai 6 ai 10 giorni, si presentano febbre generalmente elevata, cefalea persistente e importanti artralgie e dolori muscolari, che limitano molto i movimenti. Il dolore diffuso e l’infiammazione delle articolazioni rendono i pazienti immobili, in posizione antalgica. La febbre si risolve dopo 3-7 giorni dall’esordio.
Nella seconda fase della malattia, di 2-3 giorni, si presenta sporadicamente la comparsa di un esantema maculopapulare pruriginoso su tutto il corpo ed un secondo picco febbrile.
Sintomi aggravanti il quadro clinico: (1) Occasionalmente in questa fase possono aversi manifestazioni neurologiche, soprattutto nei bimbi piccoli (convulsioni), ma nel complesso il virus è poco o per nulla neurotropo. (2) Raramente si assiste al manifestarsi di miocarditi e scompenso cardiaco acuto secondario. (3) Le rare complicanze emorragiche si registrano soprattutto nelle epidemie asiatiche, ma non sono mai gravi come nella dengue: possono comparire petecchie, ma mai importanti sanguinamenti. (4) Le complicanze più gravi sono rappresentate dalla meningoencefalite e dallo shock settico da coagulazione vasale disseminata.
La Chikungunya è generalmente a decorso benigno, si autolimita, la mortalità è bassa (0.4%), ma può essere fatale, particolarmente in soggetti anziani con sottostanti patologie di base (pazienti oncologici, trapiantati, pazienti affetti da malattie croniche quali broncopneumopatia cronica ostruttiva, cardiopatie, diabete).
La malattia si risolve spontaneamente, ma i dolori articolari possono persistere per mesi. E’ essenziale un trattamento di supporto per il dolore e per la riduzione della infiammazione. La reidratazione, possibilmente infusiva con supporti di sostegno. L’utilizzo di antinfiammatori e di glutatione si è dimostrato utile per accelerare la fase di ripresa. Non sono state identificate terapie antivirali efficaci.
Controllo e prevenzione:
Per ridurre il possibile rischio di contrarre la “febbre da virus chikungunya”, come altre malattie trasmesse da artropodi, sia i viaggiatori, ma anche la popolazione che vive in aree del mediterraneo, divenute a rischio malattia per la presenza di insetti vettori e di serbatoi umani, portatori del virus, occorre ridurre l’esposizione alle punture d’insetti, applicando, per quanto possibile, tutte le misure comportamentali comunemente indicate in questi casi. L’attività degli insetti vettori del genere Aedes è generalmente presente durante tutto il giorno, ma più intensa nella fascia oraria pomeridiana e verso l’alba. Per quanto possibile, ma difficile soprattutto in corso di viaggio, è opportuno:
• indossare abiti di colore chiaro (i colori scuri ed accesi attirano gli insetti), con maniche lunghe e pantaloni lunghi, che coprano la maggior parte del corpo; e passare spray sui vestiti;
• evitare l’uso di profumi che possono attirare gli insetti;
• alloggiare in stanze dotate di impianto di condizionamento d’aria o in mancanza di questo, di zanzariere alle finestre, curando che queste siano tenute in ordine e siano chiuse;
• usare zanzariere sopra il letto, rimboccandone i margini sotto il materasso, verificandone le condizioni e controllando che non ci siano zanzare all’interno di esse. E’ utile impregnare le zanzariere con insetticidi a base di permetrina;
• utilizzare gli zampironi, presenti in commercio oppure spruzzare insetticidi a base di piretro o di permetrina nelle stanze di soggiorno o utilizzare diffusori di insetticida operanti a corrente elettrica (in tal caso bisogna informarsi del voltaggio della corrente elettrica utilizzata dal Paese in cui si soggiorna, per poter eventualmente disporre l’acquisto di adattatori o di batterie). E’ necessario, comunque, attenersi scrupolosamente alle norme indicate sui foglietti illustrativi dei prodotti repellenti, non utilizzarli sulle mucose o su regioni cutanee lese e porre particolare attenzione al loro utilizzo sui bambini.
· reti alle finestre o zanzariere nelle stanze in cui si soggiorna (meglio se impregnate con insetticidi)
· utilizzare repellenti sulle parti del corpo che rimangono scoperte, tenendo presente che il sudore ne riduce l’effetto.
UTILIZZO DI OLIO DI “NEEM COMPOSITUM” formulazione umana a base di “Azadirachta indica” e “Corymbia citriodora” per la protezione dalla puntura delle zanzare.
E’ un prodotto multiuso, naturale, sicuro, efficace, da utilizzare anche sui neonati, bambini, donne in gravidanza, soggetti iper reattivi, estratto dal frutto dell’albero di NEEM, utilizzabile anche in coloro che desiderano evitare prodotti chimici. Ha mostrato grande efficacia come repellente dalle punture degli insetti in generale, ed in modo particolare nei confronti delle punture delle zanzare. Questo prodotto è efficace anche nei confronti delle zecche. Nella formulazione per i viaggiatori questo olio, con l’ aggiunta di “essenze” quali “corymbria citrodora”, che ne potenzia l’efficacia e che ne migliora la fragranza e l’odore, possiede un utilizzo “multiplo”, nei confronti di parassiti e microbi, ed anche nelle ustioni.
UTILIZZO DURANTE I VIAGGI
RIMEDIO CONTRO INSETTI di vari tipi, ANTIZANZARE, API e VESPE, ZECCHE
RIMEDIO PER PARASSITI DELLA PELLE e CAPELLI (SCABBIA, PIDOCCHI, PULCI) ed azione ANTISETTICA contro BATTERI, FUNGHI E VIRUS);
PROTEZIONE e RIVITALIZZAZIONE CUTANEA, PROTEZIONE DEI CAPELLI; anti ustione, anti eritema solare;
- PREVENZIONE DA PUNTURE DI INSETTI ED IN PARTICOLARE DA ZANZARA
- ha una azione preventiva per le punture di tutti gli insetti ma in particolare per le punture di zanzara; allontana le zecche
- ha una forte uso: applicare sulle parti scoperte del volto, braccia e gambe, al bisogno in particolare nelle ore pomeridiane o notturne. Applicare sulla zona infiammata dalle punture per azione lenitiva ed antinfiammatoria.
- PREVENZIONE PARASSITI CUTANEI E CUOIO CAPELLUTO
- Azione anti parassitaria cutanea (scabbia, pidocchi, pulci ed altre),uccide i parassiti e toglie ponfi ed infiammazione;
uso: applicare sulle parti attaccate dai parassiti, sulle zone infiammate per le punture, sui capelli in presenza di pidocchi, anche con lo shampoo.
- Azione antisettica contro i batteri e funghi e virus presenti nelle acque utilizzate per docce, bagni, lavaggio del corpo. Azione protettiva cutanea e parti intime; molto utile nelle lavande ginecologiche (candida e batteri);
uso: in aggiunta a bagnoschiuma e shampoo (1 -2 gocce), prodotto idrosolubile;
- AZIONE PROTETTIVA CUTANEA, SOLARE ed ANTI USTIONE
- Azione protettiva e rivitalizzante cutanea da agenti atmosferici (vento, sabbia, polvere, altitudine, sole)
- Azione anti eritema solare ed antinfiammatorio dopo le esposizioni al sole;
uso: una piccola quantità in aggiunta alle creme solari; da passare dopo l’esposizione al sole come azione rinfrescante ed emolliente; da applicare sulle aree infiammate da eritema solare;
- Azione anti USTIONE: azione efficace ed immediata sulle ustioni da calore (olio, acqua, fuoco);
uso: da applicare immediatamente e continuare l’applicazione per 10 minuti; continuare ad applicare fino alla cessazione dei sintomi.
E’ possibile richiedere informazioni sul prodotto inviando una mail ad ambulatorio @ cesmet.com (con telefono, indirizzo) o telefonando alla segreteria del CESMET 06-39030481.
Nonostante i casi importati in Europa, non ci sono evidenze che indichino di limitare scambi commerciali e viaggi in queste zone, considerando il numero limitato dei casi importati e la non severità del quadro clinico. Tuttavia categorie particolari come le donne in gravidanza e le persone con malattie croniche o scarse difese immunitarie dovrebbero chiedere consigli al proprio medico sull’opportunità di intraprendere un viaggio in una zona endemica per chikungunya.
La chikungunya è tipicamente una malattia associata a viaggi, come altre malattie da artropodi. Tuttavia, poiché Aedes albopictus è presente anche in Europa e in Italia, è importante monitorare la presenza di casi sul territorio nazionale, per identificare tempestivamente, oltre i possibili casi importati, eventuali casi di trasmissione autoctona.
Non esiste allo stato un vaccino specifico nei confronti del viurs Chikungunya. Un vaccino per tale virus potrebbe essere pronto per il 2012. Ad affermarlo è Top Institute Pharma (TI Pharma) che ha deciso di investire 2,3 milioni di euro nella ricerca di un vaccino per questa malattia.
Trattamento:
Per il momento non esistono antivirali specifici ed efficaci per il trattamento contro il virus della febbre chikungunya. Quindi il virus non può essere attaccato direttamente, ma viene lentamente eliminato dalle difese naturali messe in campo dall’organismo.
Perciò la terapia è prettamente sintomatica, ossia vengono somministrati farmaci contro i sintomi acuti e cronici. L’ utilizzo di farmaci sintomatici (antipiretici, antiinfiammatori, detossificanti) è l’unica azione che può essere efficace ed aiutare il paziente per ridurre lentamente il forte stato di malessere e di dolore. L’esperienza ci dice che il riposo a letto è fondamentale per accelerare la ripresa. Una azione terapeutica importante consiste nella infusione di liquidi. Opportune infondere soluzione fisiologica ed anche reintegro di sali e lattato. Nella pratica clinica abbiamo da tempo osservato che infondere i farmaci con abbondanti liquidi favorisce e velocizza la diminuzione di febbre e dolore, e soprattutto aiuta la ripresa energetica dell’organismo.
Nelle aree endemiche e nelle zone dove si manifestano anche piccole epidemie o casi sporadici, tutte le persone affette da febbre da virus della chikungunya dovrebbero essere protette da punture degli insetti vettori, ossia dalle zanzare, per evitare che questi ultimi possano propagare l’infezione..
Diagnosi:
I metodi per la diagnosi di CHIKV possono essere sierologici o molecolari.
Non esistono, al momento attuale, kit commerciali per diagnosi di febbre chikungunya e l’allestimento dei test sierologici deve avvenire in un laboratorio a livello di biosicurezza 3 (BSL 3) dal momento che è necessario coltivare il virus.
- Saggi sierologici I test utilizzati per la diagnosi sierologica sono l’inibizione dell’emoagglutinazione (HI) e la neutralizzazione. Questi test misurano il titolo anticorpale, ma non permettono di differenziare gli anticorpi di tipo IgG da quelli di tipo IgM (indice di una infezione recente). Per effettuare diagnosi con questi test è dunque necessario disporre di due campioni di siero, uno prelevato in fase acuta ed uno prelevato in fase convalescente. Tecniche come l’ELISA o l’Immunofluorescenza (IFA) consentono di distinguere le classi di anticorpi e di definire un profilo anticorpale sia dal punto di vista qualitativo che quantitativo, permettendo di effettuare diagnosi anche in quei casi nei quali sia disponibile un solo campione di siero.
- Metodi molecolari Real time PCR, RT-PCR, Nested-PCR: sul sangue del paziente può essere eseguita la ricerca dell’acido nucleico virale, mediante l’utilizzo di primer specifici che individuino una regione conservata del genoma virale. Tali tecniche sono necessariamente allestite con reagenti preparati in laboratorio, data la mancanza di kit commerciali, e necessitano di una standardizzazione del metodo.


 l’uomo viene infettato a causa del morso del Flebotomo, la mosca del deserto (che fa parte della sottofamiglia delle phlebotominae). Queste mosche sono molto piccole, colorate e si nutrono di sangue. Vivono per lo più nella foresta, in grotte o negli anfratti delle rocce. Sia animali selvaggi che l’uomo possono fungere da vettori dell’infezione. La maggior parte delle Leishmaniosi sono originalmente infezioni di piccoli mammiferi (fungono da ‘ospiti serbatoio’) e giocano un ruolo fondamentale nella epidemiologia dell’infezione. Nelle Americhe la leishmaniosi è principalmente trasmessa dalla mosca del genere Lutzomyia, nel resto del mondo invece dal genere Phlebotomus. Le mosche si infettano nutrendosi di sangue da ‘ospiti serbatoio’ o da persone infette.
l’uomo viene infettato a causa del morso del Flebotomo, la mosca del deserto (che fa parte della sottofamiglia delle phlebotominae). Queste mosche sono molto piccole, colorate e si nutrono di sangue. Vivono per lo più nella foresta, in grotte o negli anfratti delle rocce. Sia animali selvaggi che l’uomo possono fungere da vettori dell’infezione. La maggior parte delle Leishmaniosi sono originalmente infezioni di piccoli mammiferi (fungono da ‘ospiti serbatoio’) e giocano un ruolo fondamentale nella epidemiologia dell’infezione. Nelle Americhe la leishmaniosi è principalmente trasmessa dalla mosca del genere Lutzomyia, nel resto del mondo invece dal genere Phlebotomus. Le mosche si infettano nutrendosi di sangue da ‘ospiti serbatoio’ o da persone infette. le 20 specie o più del parassita, provocano diversi tipi di sintomi, alcuni dei quali sono più comuni (febbre, malessere, perdita di peso, anemia); le forme viscerali causano anche l’ingrossamento della milza, del fegato e dei linfonodi.
le 20 specie o più del parassita, provocano diversi tipi di sintomi, alcuni dei quali sono più comuni (febbre, malessere, perdita di peso, anemia); le forme viscerali causano anche l’ingrossamento della milza, del fegato e dei linfonodi.











 Arriva l’Estate. Dopo tanto lavoro è importante godersi un viaggio in tranquillità, sicurezza e salute.
Arriva l’Estate. Dopo tanto lavoro è importante godersi un viaggio in tranquillità, sicurezza e salute.