Una nuova via contro l’antibiotico-resistenza
Una nuova via contro l’antibiotico-resistenza Leggi tutto »
Un gruppo di ricercatori italiani, guidato da Rino Rappuoli della Fondazione Biotecnopolo di Siena, ha isolato un anticorpo monoclonale capace di neutralizzare Klebsiella pneumoniae, un batterio ormai resistente a tutti gli antibiotici conosciuti. Lo studio, pubblicato su Nature, rappresenta una svolta nella lotta alla cosiddetta “pandemia silenziosa” dell’antibiotico-resistenza.
L’anticorpo agisce contro la capsula protettiva del batterio, permettendo al sistema immunitario di riconoscerlo e distruggerlo. Nei test di laboratorio e su modelli animali, ha dimostrato di bloccare completamente infezioni gravi, risultando efficace anche contro ceppi diversi ma con la stessa struttura di capsula.
La scoperta apre la strada a nuove terapie per infezioni batteriche finora considerate incurabili e consolida il ruolo di Siena e del Biotecnopolo italiano ai vertici della ricerca biomedica mondiale.
Siena apre una nuova via contro l’antibiotico-resistenza Leggi tutto »
Viaggi per lavoro o per turismo e vuoi essere sicuro e informato? Sei una azienda, un ente o una istituzione e invii personale a lavorare all’estero? oltre a leggere le informazioni sulle schede dei paesi meta dei tuoi viaggi è opportuno parlare direttamente con un medico esperto che ti consigli sulla base della sua esperienza. Rivolgiti al dr. Paolo Meo, medico tropicalista infettivologo, direttore del POLO VIAGGI Artemisia-Cesmet, con 40 anni di esperienza di lavoro in molti paesi tropicali.
Rischio malattie e comportamenti in viaggio; come affontare il viaggio e i suoi imprevisti; prevenzione e modo di evitare lo stress da viaggio e il rischio malattie; valutazione dei rischi sanitari presenti nel paese; prodotti utili per gli insetti, parassiti e questioni legate al sole da portare; profilassi farmacologica ed eventuali vaccinazioni consigliate; integratori opportuni da assumere, assistenza….questo e altro ancora …
con la CONSULENZA e le INFORMAZIONI on line prima – durante e dopo il viaggio ti informi ovunque sei, in Italia o nel mondo
per informazioni su come richiedere la consulenza: clicca qui e lascia i tuoi dati o quelli della azienda o della istituzione:

👉 Guarda il video e parti informato: la prevenzione è il primo passo per proteggere te e chi viaggia con te.
Se vuoi puoi richiedere la tua consulenza in presenza, a Roma presso gli ambulatori del POLO VIAGGI Artemisia-Cesmet in via Piave 76.
• PRIMA DI PARTIRE per turismo o missioni di lavoro:
Acquista la tua “CONSULENZA ONLINE”, ovunque ti trovi, in Italia o in qualsiasi parte del mondo; il Dott. Paolo Meo sarà a tua disposizione per fornirti informazioni, valutare i rischi del paese, fornirti e spiegarti pratiche preventive, i vaccini indispensabili, quali farmaci ed integratori . Viaggerai sicuro ed in salute.
Se hai dubbi sulla meta dei tuoi viaggi,
Se vuoi sapere come rimanere in salute ed energico durante il viaggio,
Se hai notizie e pareri discordanti su problemi che ti preoccupano riguardanti la tua meta,
Se soffri di qualche malattia e non vuoi rinunciare a un viaggio piacevole e rilassante,
Se hai sentito tante “leggende metropolitane” su eventuali medicine da assumere in prevenzione,
Se hai dubbi sulla destinazione del viaggio solo perché sono necessarie vaccinazioni,
Se hai bambini che viaggiano con te,
Se aspetti un bambino o pensi di averlo presto e vuoi viaggiare sicura,
Per ricevere informazioni e per trovare soluzioni idonee, contatta e dialoga direttamente con il Dott. Paolo Meo. Compila subito il modulo e acquista la tua consulenza.
• PRIMA DEL VIAGGIO: sei un turista o viaggi per lavoro o sei una azienda che deve inviare proprio personale per lavori all’estero: potrai effettuare la tua consulenza dialogando a distanza con lo specialista; in VIDEO WHATSAPP;
La Consulenza ha il costo di € 70,00 (clicca qui per richiederla e prendere appuntamento) oppure scrivi a [email protected]; la consulenza vale per una o più persone. (viene effettuata la verifica dello stato di salute, il controllo del libretto vaccinazioni già esistente, la possibile risposta ai vaccini ed farmaci ed altro.) Al termine della consulenza viene inviata la documentazione del paese, la ricetta dei farmaci da acquistare, e l’elenco dei vaccini indicati con la loro spiegazione.
• AL RIENTRO: se hai problemi di salute o malesseri legati al viaggio, con sintomi fisici o psicofisici quali “jet lag, alimentazione, stanchezza, ansia, contatto (e talvolta contagio) con malattie”, la visita on line con il medico specialista ha un costo di 100,00 (clicca qui e lascia i tuoi dati per essere contattato e avere l’appuntamento).
Richiedi una consulenza anche se è passato tempo dal tuo ultimo viaggio e non ti senti bene.
Il dr. Paolo Meo visita presso il POLO VIAGGI Artemisia-Cesmet in via Piave 76 Roma. In presenza potrai effettuare visite infettivologiche e tropicali, controlli e diagnosi per malaria, dengue ed altre malattie dal rientro dei viaggi.
ll dott. Paolo Meo, medico infettivologo e tropicalista ed esperto di realtà sanitarie internazionali ha lavorato e lavora in molteplici realtà tropicali di diversi continenti e soprattutto in Africa. I consigli provengono da esperienze decennali vissute nelle realtà di molti paesi.
Richiedi anche informazioni per le convenzioni con le aziende, enti o istituzioni (clicca qui)
👉 Guarda il video e parti informato: la prevenzione è il primo passo per proteggere te e chi viaggia con te.
Per ulteriori info contatta la segreteria scrivendo a [email protected]
Consulenze online viaggi Leggi tutto »
La dengue non è più solo un problema dei tropici: la zanzara Aedes sta portando questa infezione anche alle nostre latitudini. In questo video il dott. Paolo Meo, specialista del settore, spiega in modo chiaro cos’è la dengue, dove si sta diffondendo, come riconoscerla e soprattutto come ridurre il rischio durante viaggi e vita quotidiana.
Troverai consigli pratici di prevenzione personale e l’invito a rivolgerti a medici esperti per informazioni aggiornate e personalizzate.
👉 Guarda il video e parti informato: la prevenzione è il primo passo per proteggere te e chi viaggia con te.
La Dengue, un problema globale Leggi tutto »
Al 9 Ottobre 2025 i casi di Dengue nel nostro paese, sono leggi qui.…….
………………….e qui un video per scoprirne di più
La Dengue in Italia al 9 Ottobre 2025 Leggi tutto »


Leggi qui tutte le info necessarie per viaggiare
Alert, epidemie, malattie.
Nel corso del 2025 in Uganda sono state segnalate diverse epidemie, ma attualmente, OTTOBRE 2025, non risultano emergenze di dimensione epidemica generale nel Paese.
Informazioni aggiornate sulla malaria e la dengue nelle aree di Kampala, Iganga e Katatwi in Uganda:Per i mesi di settembre – novembre 2025, e tendenze per i primi mesi 2026
MALARIA
Malaria a Kampala: I casi di malaria a Kampala sono in aumento. Tra il 2020 e il 2023, i casi sono cresciuti del 29%, con un’incidenza che è passata da 165 a 233 casi per 1.000 abitanti. I gruppi più colpiti sono i bambini sotto i 5 anni e le donne adulte. Il tasso medio di positività ai test per malaria è stabile intorno al 17%. uniph
Malaria a Katatwi:Anche il distretto di Katatwi registra un’elevata incidenza di malaria, che rimane la principale causa di malattia nella zona. Recentemente, circa il 50-60% dei pazienti che si presentano nelle strutture sanitarie risultano positivi per malaria. Bambini sotto i 5 anni e donne in gravidanza sono quelli più esposti. Si stanno adottando misure preventive come la distribuzione di zanzariere impregnate e programmi di larvicidi.hejnu+1
Malaria a Iganga: Non ci sono dati diretti recenti trovati specificamente per Iganga, ma essendo una zona ad alto rischio in Uganda, è presumibile che la malaria sia presente e attiva come in altre aree rurali e peri-urbane del Paese, con particolare attenzione alla prevenzione e al trattamento.
DENGUE
Dengue: Non sono emersi dati aggiornati specifici per ottobre-novembre 2025 relativi a focolai di dengue a Kampala, Iganga o Katatwi. Tuttavia, la dengue in Uganda è presente in modo endemico e si sono registrati casi nella regione nel corso del 2024 e 2025. La sovrapposizione di sintomi con la malaria rischia di complicare la diagnosi. La dengue tende a essere meno segnalata rispetto alla malaria ma è una malattia da monitorare attentamente.academic.oup
In sintesi, la malaria è attivamente presente e in aumento in Kampala e Katatwi in questo periodo, con elevata incidenza e forti misure di controllo attivate.
La dengue è presente ma con dati meno recenti e precisi per queste aree in ottobre-novembre 2025. Per chi si reca nelle zone interessate, si raccomandano precauzioni antizanzare e test diagnostici mirati per entrambe le infezioni.
ALTRE MALATTIE EPIDEMICHE PRESENTI
La più significativa è stata l’epidemia di Mpox (vaiolo delle scimmie), che ha visto un’ampia diffusione in Africa, con nel luglio 2025 oltre 37.500 casi e 1.451 decessi in vari paesi africani, tra cui la Repubblica Democratica del Congo, Uganda, Kenya e altri.
Tuttavia, l’emergenza internazionale di Mpox è stata revocata dall’Oms a settembre 2025, poiché i casi stanno diminuendo nella regione.
Per quanto riguarda Ebola, un focolaio è stato dichiarato ufficialmente a Kampala nel gennaio 2025, con alcuni decessi e interventi di emergenza, ma non si tratta più di un’epidemia in corso attiva nel periodo attuale. L’epidemia di Ebola sarà più sotto controllo grazie agli interventi di risposta sanitaria.
Inoltre, recenti rapporti evidenziano che di nuovo si sono sviluppati casi di Mpox in Uganda fino a luglio 2025, ma la situazione sta migliorando, anche se il rischio di trasmissione comunitaria persiste in alcune aree, specialmente tra persone con HIV.
Segnali di malattie emergenti o resurrezioni di altre infezioni come il West Nile Virus non sono stati riscontrati come epidemie di vasta portata negli ultimi mesi
In sintesi, le principali emergenze sanitarie negli ultimi mesi sono state contenute o in fase di risoluzione, con Mpox rappresentando la preoccupazione più significativa fino a metà 2025. Tuttavia, il rischio di nuove epidemie o la recrudescenza di malattie come Ebola richiede una continua sorveglianza.
Il certificato di vaccinazione contro la Febbre Gialla è richiesto a tutti i viaggiatori con più di 1 anno di età.
Questo paese considera il certificato di vaccinazione per la Febbre Gialla valido per la vita (emendamento 0MS 11.07.2016). Consigliamo comunque la verifica diretta prima di partire, considerando i continui cambiamenti nei regolamenti dei singoli paesi.
La vaccinazione è raccomandata ai viaggiatori al di sopra dei 9 mesi di vita, indipendentemente dalla normativa internazionale o locale in vigore per l’ingresso nel paese. Prima della partenza informarsi presso centri specializzati sulle aree del paese a maggior rischio.
– La vaccinazione non è obbligatoria, ma va presa in considerazione a seconda del tipo di viaggio e di permanenza, ma soprattutto in base alla situazione epidemiologica del paese al momento del viaggio. La nuova formulazione “orale” del vaccino anticolera protegge ora anche dalle infezioni intestinali provocate da molti agenti enterotossici che provocano la “diarrea del viaggiatore”. Il vaccino è quindi consigliato per i viaggi in molti paesi del mondo.
Assicurati di aver effettuato tutte le vaccinazioni previste dal Sistema Sanitario Nazionale. Queste prevedono: tetano, difterite, polio, pertosse, haemophilus B, epatite B, morbillo, parotite, rosolia, varicella.
La Malaria è una malattia infettiva, acuta, presente nel paese, molto legata agli’ ambienti umidi, piovosi, alle stagioni ed alle condizioni meteorologiche. Controlla prima di partire l’itinerario del tuo viaggio e le condizioni meteo delle aree dei tuoi soggiorni. Ricorda che la Malaria è una malattia potenzialmente grave ed anche fatale. Non sottovalutarla. E’ possibile prevenirla con una attenzione al vestiario che ti copra le parti scoperte al tramonto e la notte, all’utilizzo di repellenti e all’utilizzo di adeguati farmaci per la profilassi, nelle stagioni di maggior rischio. Per approfondire leggi la scheda sulla malaria
Il rischio di malaria, principalmente da P. falciparum, esiste tutto l’anno in tutto il Paese, ivi comprese le città principali di Fort Portal, Jinja, Kampala, Mbale e parti di Kigezi. Segnalata resistenza alla clorochina e alla sulfadossina-pirimetamina.
Aggiornato a ottobre 2025
Doxiciclina, è un ottimo farmaco di scelta per i soggiorni sia in aree turistiche che in viaggi avventurosi, durante trekking e in caso di utilizzo di tende o residenze poco controllate. Farmaco per i soggiorni in residenze protette o aree di lieve rischio, sia per soggiorni a rischio elevato. Devi sapere che la “doxiciclina 100 mg”è un farmaco di scelta non solo per la prevenzione della infezione malarica ma anche per la prevenzione delle infezioni batteriche intestinali e cutanee e verso le infezioni causate da punture di zecca. Per le sue caratteristiche il farmaco è molto versatile, può essere infatti assunto per soggiorni brevissimi o brevi, alcuni giorni o settimane, ma anche nel lungo periodo,cioè per molti mesi. Ti ricordiamo che farmaci a base di tetracicline, compresa la doxiciclina, vengono assunti per oltre 1 anno da ragazzi che manifestano l’acne, cioè infezioni sul volto o tronco. Un farmaco sicuro, efficace, privo o con scarsi effetti collaterali. Ricordiamo che alle dosi di profilassi, 100 mg al giorno, gli effetti di sensibilizzazioni ai raggi solari, sono praticamente assenti. In ogni caso ricordiamo l’uso di creme solari. Farmaco di basso costo. Non è utilizzabile al di sotto dei 12 anni o in gravidanza, o in caso di allergia o intolleranza alle tetracicline. Si assume tutti i giorni, durante il pranzo, dalla entrata in area a rischio, per una settimana dalla uscita dall’area di rischio malarico.
Atovaquone-Proguanile, farmaco sul mercato da quasi 20 anni possiede ancora una buona copertura antimalarica per le forme resistenti alla clorochina, anche se sono state descritte da diversi anni forme di resistenza e di scarsa efficacia. Utile per l’utilizzo pediatrico, Utilizzato per periodi non superiori ai 30 giorni, ma utilizzabile fino a 60 giorni. Si assume una compressa tutti i giorni da 2/3 giorni prima di partire ad 1 settimana al rientro.
Meflochina, farmaco utilizzato da oltre 30 anni, Efficace in profilassi e in terapia. Efficace sia negli adulti che anche in età pediatrica. Efficacia e sicurezza dimostrata anche nelle donne in gravidanza. Utilizzabile in soggetti in buone condizioni di salute. Da non utilizzare nei cardiopatici, soggetti aritmici, neuro e psicopatici, in chi soffre di insonnia. Riferiti sintomi da irritabilità del sistema nervoso periferico e centrale. Da evitare in chi effettua immersioni, soggiorni in alta quota, voli aerei ripetuti e prolungati. Favorevole la modalità di assunzione che prevede una dose settimanale da una settimana prima di partire a 3/4 settimane al rientro.
In caso di febbre, di diarrea o comunque di malessere, è indispensabile consultare senza indugio (in caso di febbre, possibilmente entro 24 ore, per la possibilità di aver contratto la malaria, se si è di ritorno da una zona a rischio) un Medico Specialista o esperto in Malattie Tropicali.
Dai tempo al tuo organismo di ambientarsi al nuovo clima ed al nuovo ambiente. Prima del viaggio, se possibile, dedica alcune ore alla attività fisica, e abitua il tuo organismo ai nuovi ritmi durante il viaggio…leggi tutto
La vaccinazione contro la Febbre Gialla o Vaccino Antiamarillico, malattia virale acuta, che si trasmette tramite puntura di zanzara, è l’unica pratica preventiva che può essere richiesta obbligatoriamente dalle autorità sanitarie di un Paese per poter entrare attraverso i valichi di frontiera….
E’ una malattia infettiva, acuta, spesso ma non sempre febbrile, talvolta caratterizzata da pochi sintomi ma sempre con presenza di grande stanchezza, può essere fortemente debilitante, provocando anemia talvolta grave e molto spesso alterazioni metaboliche ed organiche. Appena entrati nell’organismo i parassiti colonizzano le cellule del fegato che poi vengono via via distrutte creando zone di necrosi (morte cellulale) e di fibrosi puntiforme. Alla lunga il parassita malarico crea lesioni permanenti a livello epatico. (altro che medicine contro la malaria che fanno male al fegato!).
Ricorda che la protezione dei farmaci utilizzati per la profilassi (prevenzione) è efficace e sicura. Gli eventuali effetti collaterali, raramente presenti, sono sicuramente meno dannosi, sul tuo organismo, rispetto alle conseguenze derivanti dalla malattia stessa. Tali effetti collaterali, sempre temporanei, possono dipendere da dosaggi non corretti o da intolleranze individuali. Devi temere l’azione distruttiva del parassita sul tuo organismo piuttosto che gli effetti collaterali,generalmente non pericolosi dei farmaci antimalarici.
Febbre, brividi, sudorazione, cefalea nucale, stanchezza ingravescente sono i sintomi più frequenti e caratteristici. Ma non sempre la malaria si presenta in modo così eclatante. Basta un malessere al rientro dal viaggio a far scattare l’attenzione.
FAI SUBITO GLI ESAMI DI LABORATORIO PRESSO UN CENTRO SPECIALIZZATO. TI ASPETTIAMO AL CESMET PER ESCLUDERE CON UNA VISITA E CON ESAMI MIRATI CHE I TUOI SINTOMI PROVENGANO DA UN ATTACCO MALARICO.
CHIAMA IL CENTRO CLINICO E DIAGNOSTICO TROPICALE La malaria: scheda tecnica
• le zanzare che trasmettono malattie diverse dalla malaria sono attive durante il giorno ed ovunque vi sia una raccolta di acqua dolce: indossare abiti di colore chiaro, lunghi e con maniche larghe, pantaloni lunghi e larghi, di colore chiaro, magliette o camicie con maniche lunghe e larghe e di colore chiaro da infilare nella cintura dei pantaloni….
Per prevenire l’eventuale trasmissione di malattie infettive, è opportuno nuotare esclusivamente in piscine con acqua clorata. L’acqua del mare è sicura.
Fare il bagno in acque contaminate può essere pericoloso per la pelle, gli occhi, le orecchie, le mucose della bocca, specialmente se…
E’ un insieme di sintomi che si può manifestare quando l’organismo umano, superati i 2500 metri di altitudine, non si è ancora adeguato alla nuova situazione ambientale.
Possiamo definire l’alta quota come segue…
Montagna o mare, safari e avventura o vacanza di tutto riposo, caldo o freddo: devi preparare il tuo bagaglio con cura, attenzione, senza esagerare e soprattutto prevedendo ……l’imprevedibile. Abbigliamento appropriato al clima e non dimenticando mai una piccola farmacia da viaggio.
Quando rientri da un viaggio ricorda di prenderti una pausa di un tempo sufficiente per riadattare il tuo organismo al tuo ambiente ed ai tuoi ritmi di vita. Stanchezza, malessere, senso di vuoto, scarsa capacità alla concentrazione….
Capitale: Kampala
Moneta: Franco del Burundi
Fuso orario: GMT+3
Storia,Economia,Cultura: https://www.cia.gov http://www.britannica.com
Sicurezza: www.viaggiaresicuri.it www.dovesiamonelmondo.it
Uganda – Scheda Paese Leggi tutto »
L’influenza sta arrivando. La aspettiamo in Italia nella seconda parte del mese di dicembre e durerà fino a febbraio inoltrato. La vera influenza sarà quindi presente in un periodo ben definito. Anche quest’anno, come sempre, i giornali stanno dando l’allarme e ci avvisano che, in coincidenza dei primi venti che scuotono le foglie degli alberi nei viali, il virus dell’influenza ritorna ad affliggere l’umanità nel nostro emisfero. Anche quest’anno riprenderanno le solite raccomandazioni: è bene vaccinarsi; è bene prendere gli antibiotici; è bene seguire i rimedi della nonna. A noi però, gente comune, cosa conviene sapere veramente, per farci un’opinione corretta e proteggerci al meglio da questa infezione?
Il CESMET risponderà a questa esigenza e seguirà il problema dell’influenza durante tutto il periodo dell’epidemia. Ci saranno aggiornamenti sulla evoluzione della epidemia in Italia ed in Europa ed informerà il suo pubblico di internauti sulle nozioni da considerare già acquisite e sulle novità che si affacceranno.
Per cominciare 👉 Guarda il video e scopri le strategie più efficaci per difendere te stesso e chi ti sta vicino, e poi ecco le FAQ che più frequentemente ci vengono rivolte:
Caro lettore ricorda: “Ci sono tante diverse malattie respiratorie d’inverno. Queste malattie sono portate dall’aria fredda, e da un ambiente autunnale ed invernale aggressivo nei confronti del nostro sistema respiratorio. Qualcuno aggiunge che le nostre vie respiratorie in questa stagione hanno una tendenza ad irritarsi ed a favorire l’attecchimento dei virus. Ma queste malattie respiratorie, sia delle alte vie che delle basse, non sono solamente di origine influenzale. L’influenza è solo una malattia provocata da un virus ben preciso ed è presente solamente in un periodo ben definibile (dicembre – febbraio). Tanto per chiarire pensa quanti altri virus causano problemi respiratori che sono simili all’influenza: il virus respiratorio sinciziale; gli adenovirus; i rinovirus; i coronavirus, gli enterovirus e così via.
Nel periodo autunnale in cui non è presente una epidemia ben definita, quella influenzale, è praticamente impossibile distinguere una forma virale dall’altra, perché le sintomatologie all’esordio sono simili. Solo per l’influenza, causata dal virus influenzale vero e proprio, sappiamo che si rivela e si manifesta come una malattia respiratoria più grave e più importante delle altre, che dura più tempo e presenta un numero di complicazioni maggiore, ma sappiamo anche precisamente il suo periodo di comparsa. Per distinguere la malattia influenzale dalle altre forme virali sono stati proposti dagli scienziati dei parametri in base ai quali è possibile porre una diagnosi iniziale che poi necessita, se lo si ritiene opportuno, di una conferma in laboratorio. Pertanto la cosa migliore, se sospettiamo di avere contratto l’influenza, è avvisare il proprio medico del nostro stato di malessere oppure chiedere una visita ai medici del CESMET, per una valutazione se è il caso di richiedere un test di conferma. E’ chiaro che la malattia influenzale potrà essere sospettata solamente quando il virus influenzale giungerà in Italia. Questo è previsto tra metà dicembre fino a febbraio inoltrato. Tutte le forme così dette influenzali presenti in Ottobre, novembre e primi giorni di dicembre non sono da considerare influenza propriamente detta.
Bisogna tenere conto di alcuni fatti ben precisi. L’influenza da “virus influenzale” si diffonde velocemente in comunità chiuse, (scuole, uffici, ospedali,case di cura, carceri etc.). Ogni gocciolina di saliva o proveniente da sternuti, che un individuo infetto emette respirando, contiene da 100.000 a 1.000.000 di virioni (che parolona!). I virioni? Tali microscopiche particelle infettanti, cioè il virus vero e proprio, (di questo si tratta) si depositano nell’ambiente (sulle maniglie delle porte in un ufficio ad esempio!) e possono risultare facilmente infettanti se inalate, dopo che le abbiamo toccate.
Si ritiene che bastino 10 particelle di virus che arrivano in contatto con le nostre mucose del naso o della bocca per infettarci o infettare un’altra persona! L’individuo infetto dal virus influenzale può trasmettere la malattia a tutti quelli che lo circondano dal giorno prima dell’inizio dei suoi sintomi fino a cinque giorni dopo l’insorgenza della sintomatologia. Quindi ciascuno di noi può diventare in famiglia, in ufficio, in metropolitana, al cinema, nei grandi magazzini un soggetto infettante. Ma non solo: sappiamo che durante l’epidemia influenzale il 30-50% dei casi decorre in maniera asintomatica. E chi ha il virus ma non ha i sintomi è in ogni caso un diffusore di particelle virali.
Pertanto nei mesi dell’epidemia (tra dicembre e febbraio) ognuno di noi ha la quasi certezza di venire in contatto con il virus e sviluppare la malattia.
Ti consiglio non di murarti vivo ma, in una parola, di effettuare prevenzione.
Per fare prevenzione nei confronti dell’influenza, la vera malattia influenzale, presente da metà dicembre a tutto febbraio, ciascuno di noi deve fare due cose:
È stato scientificamente dimostrato che gran parte della diffusione del virus influenzale avviene toccando con le mani oggetti inavvertitamente contaminati da starnuti di altre persone infette e portando il virus con le mani a contatto delle mucose del naso o della bocca. È quindi fondamentale per interrompere questa catena di trasmissione della malattia influenzale, che ciascuno di noi partecipi, col modesto sacrificio, alla pratica di lavarsi le mani frequentemente. Un altro consiglio è quello, per quanto possibile di cercare di evitare i luoghi chiusi ed affollati durante il periodo epidemico. Se poi non ti sei vaccinato e ti ammali il consiglio è quello di rimanere a casa per alcuni giorni. Avrai la possibilità di curarti meglio e limiterai al massimo le possibilità di trasmettere il virus ad altri individui. A proposito ricordati di coprirti la bocca ed il naso quando starnutisci.
Si tratta di distinguere di quale genere di rischio parliamo. Per quanta riguarda le probabilità di ammalarsi, si.
E’ questione di protezione immunitaria. Le fasce di popolazione più giovani hanno le probabilità più alte di contrarre l’influenza. I giovani adulti hanno una alta frequenza di ammalare. Però in termini di gravità le probabilità di sviluppare una forma grave o delle complicazioni (polmoniti gravi, insufficienza renale, altre cose) sono maggiori per i soggetti anziani (sopra i 65, diciamo), perciò cerca di convincere i tuoi anziani a vaccinarsi. Sarà meglio per tutta la famiglia, ma soprattutto per loro.
Il costo medio di ogni ricovero per sindrome influenzale è piuttosto elevato: costo del posto-letto, del personale, degli antibiotici, degli antivirali, di tutte le altre terapie di supporto. Di eventuali ricoveri (speriamo di no) in reparti di terapia intensiva. Moltiplicalo per il numero di persone che verranno ricoverate per questo motivo, e siamo nell’ordine delle centinaia di migliaia, anzi di milioni di Euro. Ti renderai facilmente conto della forte spesa sociale costituita dall’influenza stagionale. Inoltre in questo numero non abbiamo preso in considerazione la spesa dovuta alla perdita di giornate di lavoro.
Siamo in crisi economica, come giustamente dici tu, e non possiamo permetterci di rallentare ulteriormente lo sviluppo economico, limitando la disponibilità della forza lavoro. Alcuni studiosi infatti hanno stimato che il virus influenzale porta ad una perdita di produttività: infatti in media ogni caso di influenza fa perdere 4,78 giorni di lavoro/scuola; si stima che nella stagione 1998/99 si siano persi in Italia circa 48 milioni di giorni lavoro/scuola. Una cifra sconvolgente! Forse vale la pena fare qualche cosa!
I vaccini vengono rinnovati ogni anno. In tutto il mondo le case di produzione dei vaccini ricevono dagli studiosi e dai centri ufficiali le caratteristiche del nuovo tipo di virus su cui produrre il nuovo vaccino. Quindi ogni anno i vaccini vengono prodotti sapendo molto bene le caratteristiche ed il tipo di virus che troveremo in circolazione quest’anno in Italia e nel mondo. E sai perché lo sappiamo? lo sappiamo perché la malattia influenzale non è finita l’anno scorso a febbraio, ma questa estate ha continuato a circolare in America del Sud, in Australia, e i locali medici competenti hanno continuato a studiarlo, isolarlo e hanno fornito a noi dell’emisfero Nord tutte le informazioni che servono per proteggerci. Infatti ti posso già annunciare, e te lo dico giusto perché so che sei una persona curiosa, che il prossimo vaccino, che è già in commercio, è composto da una miscela di 4 ceppi differenti:
Le varianti, come le avrebbe dovute chiamare il tuo amico, in realtà sono già state previste nella nuova formulazione del vaccino e tutto andrà per il meglio.
Concludo e ti saluto.
Ciao. Alla prossima visita al sito del CESMET!
Domande frequenti sull’influenza Leggi tutto »
La “Febbre da virus Dengue” negli ultimi decenni si è diffusa a macchia d’olio e si è imposta come emergenza di sanità pubblica nella maggior parte dei paesi tropicali. In Africa si è diffusa in modo particolare negli ultimi venti anni, in Asia ed in particolare in America Centrale e Meridionale è una malattia endemica con epidemie diffuse. (OMS 2021 CLICCA)
Centrale e Meridionale è una malattia endemica con epidemie diffuse. (OMS 2021 CLICCA)
Il “vettore primario” per questa malattia è una zanzara, la Aedes, che è diffusa nella maggior parte dei paesi equatoriali e tropicali, e si sviluppa in particolare nelle zone urbane dove gli abitanti sono molto suscettibili all’infezione. Il processo di urbanizzazione selvaggia degli ultimi trenta anni ha lasciato, in molti paesi depressi, la popolazione con sistemi fognari a cielo aperto, con discariche inserite nel tessuto urbano, con sistemi per la raccolta delle acque non controllati e con dispersioni di acqua in altissime percentuali. Acquitrini e paludi all’interno e nelle periferie delle città costituiscono un polmone per la presenza delle zanzare. Tutto questo ha consentito la formazione di ambienti favorevoli all’insediamento ed alla crescita del vettore, velocizzando in questo modo la diffusione dell’infezione.
———————————————————————————————————————————————————————
INFO URGENTE PER CHI VIAGGIA:
EMERGENZA DENGUE CLICCA QUI
PRENOTA IL VACCINO PER LA DENGUE
———————————————————————————————————————————————————————
Come si manifesta la febbre emorragica da virus Dengue?
La “febbre da virus dengue” può manifestarsi in diversi modi. Da una “infezione asintomatica” ad una “malattia lieve” fino a “forme gravi e mortali” . Studi epidemiologici in diversi continenti stimano che una su quattro infezioni manifestino sintomi. Oltre il 70% delle persone punte da zanzare con il virus si infetta in modo asintomatico. Un 30/35 % delle persone infettate manifesta la malattia e i sintomi si manifestano in modo acuto da lievi a moderati e generalmente aspecifici.
Quanti sono i tipi del virus della Dengue

Quattro sono i tipi di virus della Dengue. Ogni tipo induce una immunità specifica verso il proprio ceppo, di lunga durata, ma che non copre gli altri tipi. Quindi le persone possono essere infettate dal virus della dengue fino a quattro volte.
Le forme gravi e talvolta mortali di malattia incorrono in circa 1 paziente su 20.La seconda infezione da DENV è un fattore di rischio per la dengue grave.
Come viene classificata la DENGUE secondo OMS
La febbre da virus dengue è classificata in (1) dengue o (2) dengue grave;
(1) DENGUE è definita, in una persona febbrile che ha viaggiato o vive in un’area endemica, da una combinazione di 2 o più dei seguenti segni o sintomi. Tra i sintomi: la nausea, il vomito, eruzioni cutanee, dolori, un test del laccio emostatico positivo, la leucopenia. Tra i segni: dolore o dolorabilità addominale, il vomito persistente, l’accumulo di liquidi, il sanguinamento della mucosa, la letargia, l’irrequietezza e epato e splenomegalia.
(2) DENGUE GRAVE è definita con uno qualsiasi dei seguenti sintomi: una grave perdita di sangue che porta a shock, l’accumulo di liquidi con distress respiratorio; un grave sanguinamento; una grave insufficienza epatica con transaminasi ad oltre ≥1.000 UI/L, alterazione della coscienza, una insufficienza cardiaca.
Questa classificazione sostituisce la precedente in uso dal 1975 al 2009 classificate come (1) febbre da dengue; (2) febbre emorragica dengue (DHF);
(3) sindrome da shock dengue – la forma più grave di DHF.
CARATTERISTICHE DEL VIRUS DELLA DENGUE
Il virus della “febbre da Dengue” appartiene alla famiglia dei Flaviviridae ed ha quattro principali sierotipi simili tra loro:
DEN-1, DEN-2, DEN-3, and DEN-4. Questi sierotipi del virus hanno un genoma ad RNA.
Quali altri virus oltre quelli della DENGUE fanno parte della famiglia dei “FLAVIVIRUS” ?
Fanno parte della “famiglia dei Flavivirus” altri virus causa di febbri emorragiche presenti prevalentemente in aree tropicali quali: la febbre gialla; l’encefalite di Saint-Louis (america del nord); l’encefalite giapponese; West Nile virus; .
Tutte queste malattie sono trasmesse da artropodi, soprattutto da diversi tipi zanzare e da zecche degli animali, e questi virus causa di queste malattie sono anche denominati Arbovirus ossia “arthropod borne virus” – virus trasmesso da artropodi.
I Flavivirus sono virus con genoma ad RNA a singolo filamento positivo appartenenti alla famiglia Flaviviridae. La struttura di questi virus è formata da alcune molecole proteiche più esterne che formano il “pericapside”; molecole proteiche più interne che formano il ”capside”; ed una sola molecola ad RNA, con un senso di lettura 3′ – 5′.
I “VIRIONI” della DENGUE sono di forma sferica, dotati di un “PERICAPSIDE” della dimensione di 50 nm. Questo ricopre un “NUCLEOCAPSIDE” della dimensione di 30 nm di diametro.
 [A] “capside virale”: composto da tre proteine strutturali: (1) proteine di rivestimento esterno (E); (2) proteine del capside (C); (3) proteine di membrana interna (M);
[A] “capside virale”: composto da tre proteine strutturali: (1) proteine di rivestimento esterno (E); (2) proteine del capside (C); (3) proteine di membrana interna (M);
Le glicoproteine E, envelope esterno, svolgono un ruolo centrale nella biologia delle infezioni. Costituiscono il legame del virus con la superficie cellulare e favoriscono la penetrazione nella cellula bersaglio. Questa proteina esterna (E) è il “bersaglio” della risposta immunitaria dell’organismo ospite. La proteina E è costituita da 500 aminoacidi con tre “domini antigenici”.
Le 90 glicoproteine dimeriche (E) sono coinvolte nell’attacco e nella penetrazione nella cellula. Sono disposte parallelamente alla superficie del virione, formando una struttura “a spina di pesce” a simmetria icosaedrica. Questa struttura è stata sudiata nel VIRUS della DENGUE tipo 2, nell’ WNVirus nel virus dell’encefalite trasmessa da zecche. La conferma di questa struttura è arrivata dalle immagini ottenute con la microscopia crioelettronica.
La proteina interna del capside ( C ) è una proteina strutturale ed ha la funzione di assemblare insieme le parti del virione.
I virioni del virus DENGUE si assemblano nel citoplasma cellulare, via via che vengono prodotte le proteine dai ribosomi delle cellule ospiti e, migrando verso la periferia della cellula, vengono liberati all’esterno per un processo di “gemmazione” della membrana cellulare.
Il genoma del virus della Dengue contiene 11.000 paia di basi e la sua funzione è quella di passare l’informazione per codificare (realizzare) 3 proteine strutturali esterne e 7 proteine non strutturali ma funzionali per la replicazione virale: (a) tre proteine che costituiscono la struttura esterna del virus, il virione, ossia il “cappotto / corpo del virus”,
Le proteine sono denominate(C; prM; E); (B) sette diverse proteine che vengono prodotte e rilasciate nella cellula ospite (umana) e consentono la replicazione e la moltiplicazione dei virus (figli) (NS1, NS2a, NS2b, NS3, NS4a, NS4b, NS5)
I cinque sierotipi della famiglia della DENGUE
Il virus DENGUE esiste in cinque diversi sierotipi, denominati DENV-1, DENV-2, DENV-3, DENV-4 e DENV-5.
Ognuno dei diversi tipi di virus dengue può causare la malattia febbrile con sintomi acuti, causati da una risposta infiammatoria dell’organismo, spesso abnorme ed anche pericolosa per l’organismo stesso.
Come avviene la trasmissione della DENGUE?
Il “virus della febbre da virus dengue” è caratterizzato da due trasmissioni con differenti caratteristiche:
[A] La “trasmissione / diffusione silvestre”, ossia in ambiente rupestre, di savana e di foresta, utilizzando vettori, in questo caso zanzare denominate AEDES, che succhiano sangue di “primati”, in questo caso di scimmie. Si ritrovano nelle foreste del Sud-est asiatico, dell’Africa e della America Latina. Nelle aree rurali delle aree tropicali la trasmissione avviene solitamente tramite puntura da parte di Aedes aegypti e altri tipi tra i quali Aedes albopictus denominata anche zanzara tigre dalle caratteristiche zampe a strisce di tigre. “Aedes albopictus” è la zanzara che si è anche diffusa in Europa, ed in particolare nel bacino del mediterraneo.
[B] La “trasmissione cittadina” avviene tramite Aedes aegypti. Il ciclo vitale del vettore nelle aree urbane è caratterizzato da trasmissione “interumana”. L’ospite è l’uomo, che viene punto dalla zanzara, che trasmette il virus ad un altro individuo. La crescita incontrollata delle città, con ambienti favorevoli alla riproduzione delle zanzare, nelle aree endemiche per la dengue ha portato a un aumento esponenziale delle epidemie e della quantità di virus circolante. I cambiamenti climatici, con l’innalzamento delle temperature e dell’umidità, e il diffondersi di aree acquitrinose, hanno permesso la diffusione anche in zone originariamente risparmiate, in particolare nelle aree rivierasche dei paesi mediterranei, ma sempre più anche nelle aree interne e continentali. Queste condizioni hanno permesso ormai la diffusione di Aedes in molte zone d’Europa, con l’insorgenza di piccoli focolai, anche autoctoni di febbre da Flavivirus, ed in particolare casi di Dengue. e potrebbe, in futuro, rappresentare una minaccia per l’Europa.
L’infezione di un sierotipo causa una malattia simile agli altri, ma conferisce una immunità specifica per il sierotipo, a vita, ma non protegge dall’attacco degli altri sierotipi, che possono indurre una malattia simile, e indurranno un ulteriore immunità specifica solo per il sierotipo in questione. Per questo meccanismo di protezione immunitaria sierospecifica, ci si può infettare di DENGUE solamente 4 volte. Ma le reinfezioni possono essere pericolose per reazione immune ed infiammatoria abnorme.
E’ noto che la forma severa, pericolosa e particolarmente acuta, dovuta ad una risposta immune abnorme avviene in caso di infezione secondaria in individui che prima hanno avuto infezione da DENV-1 e che in seguito vengono infettati da DENV-2 o DENV-3. Una altra reazione particolarmente grave può avvenire in persone infettate prima da DENV-3 e poi reinfettate con DENV-2.
Le zanzare trasmettono con la loro puntura il virus agli esseri umani dopo che hanno punto una persona infetta, infettandosi. La trasmissione non è quindi diretta uomo – uomo, ma sempre attraverso la puntura di un vettore.
Il virus entra nel circolo, depositato dalla zanzara, che lo inocula nel microcircolo del sottocutaneo. Circola per 2-7 giorni ed è in questo periodo che un’altra zanzara, pungendo l’uomo infetto, può prelevarlo e trasmetterlo ad altri soggetti. Il “virione con genoma a RNA” entra nel microcircolo viene assorbito e va a legarsi alle membrane delle cellule endoteliali dell’ospite stesso. Sebbene il recettore al quale si legano dia luogo ad endocitosi, il virione comunque rimane momentaneamente bloccato nella cellula ospite all’interno di una vescicola.
Le membrane della cellula ospite sono associate a glicoproteine che contengono una regione che media la fusione fra la membrana cellulare e l’involucro esterno del virione. Questa fusione avviene in ambiente acido. Una volta avvenuta la fusione il virus perde il rivestimento esterno e comincia la traduzione del suo genoma. Si ha quindi la produzione di proteine virali fra il reticolo endoplasmatico e l’apparato del Golgi dove eventualmente le membrane cominciano a riavvolgere il genoma virale dando luogo alla moltiplicazione virale. I virioni si accumulano quindi nelle cellule dell’ospite. Lo step finale del ciclo vitale si ha con la fusione delle vescicole contenenti i virioni con le membrane delle cellule plasmatiche. A questo punto le particelle sono rilasciate e libere di infettare altre cellule.
I Flavivirus in genere, ed il virus della Dengue in particolare, vengono trasmessi attraverso la puntura di diversi tipi di zanzare. Il vettore principale per la Dengue è la zanzara del genere Aedes aegypti. Anche A. albopictus, che si è diffusa in Europa negli ultimi decenni, può trasmettere il virus. Questo tipo di zanzara si nutre di sangue umano prevalentemente di giorno, ma questa non è una regola fissa. Troviamo zanzare del genere Aedes attive anche durante il crepuscolo e la notte. Aedes, durante il pasto, punge individui, alcuni dei quali possono essere infetti del virus in questione. La zanzara, quindi, si infetta, e può rimanere infetta tutta la vita, diventando la causa di molteplici infezioni. Ogni esemplare vive dalle 2 alle 4 settimane, pungendo ed ovideponendo numerose volte. La zanzara può infettare un individuo per ogni puntura. E’ oramai accertato che le zanzare femmine possono trasmettere l’infezione alle generazioni successive. Difatti può passare il genoma virale alle larve amplificando il numero di zanzare adulte infette.
L’uomo diventa quindi l’ospite con cui infettarsi o da infettare. L’uomo funge quindi da ospite amplificatore della diffusione del virus. Anche alcuni tipi di scimmie possono essere infettate dalla puntura della zanzara Aedes e a sua volta infettare scimmie e uomini.
La zanzara del genere Aedes è uno dei pochi vettori che utilizza non solamente le raccolte di acqua per la crescita delle larve, ma anche un ambiente umido e questa caratteristica moltiplica in modo esponenziale la crescita e la diffusione di questo tipo di zanzare.
Porta di ingresso del virus e attività nelle cellule interne del sistema istio – linfocitario
La porta di ingresso dei Flavivirus, ed in particolare dei virus della Dengue è la CUTE. Il virus penetra insieme alla saliva dell’insetto. Nel sottocute e nel derma circostante all’inoculo i leucociti accorsi per difendere l’organismo da un nemico esterno, vengono attaccati. Il virus aderisce alla loro parete e penetra al loro interno, riproducendosi velocemente. In particolare il virus dengue aderisce allele cellule di Langerhans, cellule dendritiche, dalla forma a stella, che sono abbondanti nella cute, sotto cute e derma ed anche in alcune mucose. Hanno la funzione di attivare ed amplificare il sistema difensivo chiamando altri tipi di globuli bianchi con i loro segnali chimici. I Flavivirus (Dengue) entrano in questi tipi di globuli bianche attraverso il processo di endocitosi mediato dal contatto e interazione tra proteine virali e proteine specifiche presenti nella membrana cellullare. Queste proteine sono la lectina DC-SIGN, la CLEC5A ed il complesso proteico che forma il recettore per il mannosio. Questa interazione tra proteine virali e proteine della cellula di Langerhans o di altri GB quali monociti e macrofagi, consente l’entrata nella cellula stessa. Il virus comincia a replicare all’interno della cellula all’interno di microvescicole adese al sistema reticolo endoplasmatico. Qui il genoma virale ad RNA viene copiato attraverso l’attivazione dei ribosomi, e comincia la produzione delle che verranno assemblate nell’apparato di Golgi cellulare dove avviene la maturazione e la costituzione dei nuovi virioni che escono dalla cellula mediante il processo di esocitosi. Questi leucociti infetti si spostano verso i linfonodi più vicini.
Le membrane della cellula ospite sono associate a glicoproteine che contengono una regione che media la fusione fra la membrana cellulare e l’involucro esterno del virione. Questa fusione avviene in ambiente acido. Una volta avvenuta la fusione il virus perde il rivestimento esterno e comincia la traduzione del suo genoma. Si ha quindi la produzione di proteine virali fra il reticolo endoplasmatico e l’apparato del Golgi dove eventualmente le membrane cominciano a riavvolgere il genoma virale dando luogo alla moltiplicazione virale. I virioni si accumulano quindi nelle cellule dell’ospite. Lo step finale del ciclo vitale si ha con la fusione delle vescicole contenenti i virioni con le membrane delle cellule plasmatiche. A questo punto le particelle sono rilasciate e libere di infettare altre cellule.
I leucociti infetti producono interferone e altri fattori e molecole scatenanti diversi processi che inducono aumento della temperatura (febbre), dolore, brividi e sudorazione ed altri sintomi simil-influenzali.
Il sistema immunitario produce tra le diverse molecole gli interferoni molecole particolarmente attive nella difesa da infezioni virali. I sierotipi di dengue virus hanno la capacità di diminuire o neutralizzare l’efficacia dell’interferone. Sempre gli interferoni attivano i linfociti T contro i virus, ed anche i linfociti B che inducono la produzione di anticorpi contro gli antigeni virali. Alcuni tipi di virus Dengue riescono ad eludere questi meccanismi di attacco delle cellule difensive. I virus vengono trasportati lontano dai lisosomi del fagocita, evitano la distruzione e continuano a replicare.
Infezioni particolarmente gravi e con elevata presenza di virus coinvolgono anche il fegato il midollo osseo, causando lesione delle cellule del parenchima ma anche dell’endotelio dei vasi capillari. La replicazione del virus nelle cellule del midollo osseo altera i processi di emopoiesi. A causa di una alterazione del processo di maturazione delle cellule ematiche, diminuiscono in quantità e funzionalità le piastrine, causando piastrinopenia, più o meno accentuata, responsabile delle emorragie tipiche della dengue.
Sempre per effetto di alcuni meccanismi che esitano in lesioni cellulari da parte dei virus, in particolare a livello dell’endotelio vascolare, con aumento della permeabilità vascolare, passato il rapido periodo febbrile tipico dei primi giorni, si può verificare un versamento pleurico (accumulo di liquidi nel torace) o la presenza di ascite nell’addome. L’esito è una diminuzione dei liquidi intravascolari con ipovolemia e scarsa perfusione degli organi vitali.
Le manifestazioni di Dengue Grave, con shock o febbre emorragica si presentano in meno del 5% dei pazienti ed in particolare in coloro che sono infettati una seconda volta da un diverso sierotipo del dengue virus.
Incubazione
L’incubazione della malattia varia da 2 a 15 giorni con un esordio che generalmente è improvviso, acuto o iperacuto.
Agg. Del maggio 2023
Secondo l’Organizzazione Mondiale della Sanità la “Febbre da virus Dengue” causa oltre 100 milioni di casi ogni anno in tutto il mondo. La Dengue è diffusa in tutto il Sud – Est Asiatico, nell’Asia sud – Occidentale, in Oceania ed in Estremo Oriente. E ‘presente anche nel continente africano.
Si stima che oltre il 50% della popolazione mondiale sia a rischio di questa malattia.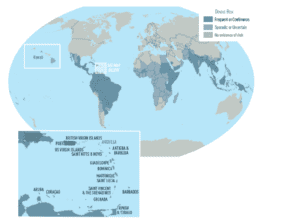
Attualmente oltre 4 miliardi di persone vivono in 125 Paesi a rischio Dengue.
La diffusione della dengue continua ad aumentare ed in molte regioni tropicali nel post pandemia del Covid-19 ha avuto un aumento anche del 500/700%. Numeri impressionanti, anche per l’incuria a cui è stato abbandonato l’ambiente dove si riproducono gli insetti.
L’Europa ed in particolare i paesi del bacino del mediterraneo, a causa dei cambiamenti climatici, per aumento di calore, umidità e piogge, ma anche per l’aumento di spostamento di merci e persone sono diventati paesi a rischio Dengue, dove già si presentano sporadici focolai autoctoni della malattia.
Quasi la metà della popolazione mondiale, circa 4 miliardi di persone, vive in aree a rischio dengue, e i numeri sono in aumento. La “febbre virale da Dengue” è diventata una delle principali cause di malattia nelle aree a rischio . Nell’Unione Europea la febbre dengue si verifica in modo sporadico, soprattutto nell’Europa continentale dove non esistono le condizioni per una diffusione della malattia con casi autoctoni. I paesi che si affacciano sul bacino del Mediterraneo, per le loro caratteristiche climatiche, sono diventati sede di focolai che si sviluppano indipendentemente dall’importazione dei casi dal tropico.

I casi in Europa derivano da viaggiatori che tornano dopo essersi infettati dal tropico. Dal 1999, il Network europeo per la sorveglianza delle malattie infettive da importazione (TropNetEurop) ha riportato oltre 2000 casi di dengue fra i viaggiatori europei. Nella maggior parte dei casi, le infezioni sono state contratte, nell’ordine, in India, in Thailandia, in Indonesia, in Messico e in Brasile. Secondo il documento dell’Ecdc “Dengue Ferver: Short epidemiological update, 2009”, tra gennaio e giugno 2009 sono stati riportati nelle Americhe un totale di 480.909 casi di dengue, compresi 7.547 casi di febbre emorragica da dengue, con 189 decessi; il 91% di questi casi è stato segnalato in Argentina, Bolivia, Brasile e Colombia.
La dengue è emersa come un problema globale a partire dagli anni ’60. La malattia è comune in molte destinazioni turistiche popolari nei Caraibi (incluso Puerto Rico), nell’America centrale e meridionale, nel sud-est asiatico e nelle isole del Pacifico. Negli Stati Uniti, casi locali e una limitata diffusione della dengue si verificano periodicamente in alcuni stati con climi caldi e umidi e zanzare Aedes.
Chiunque viva o viaggi in un’area a rischio dengue è a rischio di infezione.
La “febbre da Dengue” si presenta con una sintomatologia acuta, generalmente violenta, dalle caratteristiche simil-influenzali. La malattia nei bambini si può manifestare con caratteristiche simili ad una influenza forte con presenza di roseole e reazioni cutanee. Gli adolescenti e gli adulti, rispetto ai bambini, presentano sintomi più leggeri con febbre più contenuta. La malattia si manifesta con sintomi caratteristici quali rialzo di temperatura elevato, mal di testa, dolore agli occhi, dolore anche importante alle articolazioni e ai muscoli. Talvolta manifestazioni eritematose esantematiche cutanee.
La persona che si infetta con un sierotipo, per la prima volta, si immunizza verso questo sierotipo e difficilmente ammala una seconda volta. Ma se la stessa persona contrae una infezione con un sierotipo differente, è elevata la possibilità di una manifestazione di “febbre emorragica da Dengue (DHF)”. Questa forma morbosa, causata dall’infezione di un secondo tipo di dengue, differente dal primo, può portare manifestazioni particolarmente acute e talvolta fatali.
La DHF è caratterizzata da febbre acuta ed elevata; dolori generalizzati particolarmente violenti; manifestazioni cutanee caratterizzate da fenomeni emorragici petecchie, ecchimosi, porpora, epistassi, sanguinamento delle gengive, ematuria o risultato positivo del test del laccio emostatico.
Tra gli altri sintomi è frequente l’ingrossamento del fegato e della milza (epato-splenomegalia); collasso del sistema circolatorio.
Caratteristica della malattia la presenza di una febbre in rapida crescita; brividi squassanti e talvolta sudorazione; eritema facciale è l’inizio degli episodi anche di piccole emorragie puntiformi, dovute al crollo delle piastrine. La febbre con picchi fino a 41°C può durare generalmente dai 2 ai 5 giorni. Spesso, soprattutto nei bambini piccoli è accompagnata da convulsioni squassanti.
Senza un adeguato trattamento sintomatico, per il controllo dello stato di shock, il collasso cardio – circolatorio, la diminuzione drastica di piastrine, il paziente può morire in 12-24 ore.
Il tasso di letalità della “febbre emorragica da dengue” a una incidenza talvolta superiore al 30%;
I decessi sono prevalenti nei neonati < 1 anno.
Sono da considerare “segnali premonitori” di un peggioramento della febbre da dengue verso una forma grave o da DHF, quei sintomi che si manifestano al termine della fase febbrile (tardiva), durante il periodo della defervescenza della febbre (verso il 5° giorno di sintomi). Il manifestarsi di vomito persistente, dolore addominale importante, spesso crampiforme, edema diffuso per accumulo di liquidi; sanguinamento delle mucose e una ingravescente difficoltà respiratoria. Tutti questi sintomi in fase tardiva accompagnati talvolta da letargia o irrequietezza, tendenza all shock, ingrossamento rapido del fegato con dolenzia in ipocondrio destro e segni di emoconcentrazione, ossia aumento dell’ematocrito costituiscono elementi di aggravamento e segnali di avvertimento di evoluzione verso gravi forme da DHF.
La prima diagnosi o sospetto diagnostico è sempre clinico. I sintomi possono essere confusi con quelli del tifo esantematico da zecche (Rickettsie); della febbre da zecche del Colorado, della febbre gialla e con altre febbri emorragiche.
Il sospetto clinico per malattia da Dengue virus va considerato in tutti coloro che denunciano sintomi clinicamente compatibili e che vivono o hanno viaggiato nelle 2 settimane prima dell’esordio dei sintomi in aree endemiche per la malattia.
In chi presenta in modo acuto febbre, mal di testa, dolori muscolari e talvolta eruzioni cutanee al rientro da paesi endemici dell’area tropicale e subtropicale, va posto il sospetto diagnostico e prescritti esami per confermare la diagnosi.
Anche per Dengue virus, come per molti altri virus, il test PCR o di “amplificazione degli acidi nucleici” risulta essere il “gold standard per la diagnosi di laboratorio”.
Il siero su cui eseguire la PCR deve essere raccolto nell’individuo dal momento dell’insorgenza dei sintomi fino al 7° giorno dopo l’esordio della malattia.
La conferma della presenza del virus può essere effettuata da un singolo campione di siero rilevando:
La positività del test eseguito con le due metodiche è la conferma di laboratorio della malattia da dengue nei pazienti con una storia clinica o di viaggi effettuati in aree endemiche. La positività è presente nei primi 7 giorni di malattia ma può perdurare, soprattutto per la NS1, fino a due settimane.
I test sierologici (o da studio del siero) identificano la presenza di
Quindi in caso di sintomi sospetti e provenienza da zone endemiche il paziente deve essere sottoposto a test molecolare o antigenico (RT-PCR o NS1) e a test sierologico per la ricerca degli anticorpi (IgM).
Tuttavia, per il fenomeno della reattività crociata con altri flavivirus come Zika, l’interpretazione dei risultati e l’identificazione del virus, causa della malattia, può essere difficile.
La positività delle IgM in un campione di siero dimostra e conferma una recente infezione da virus della dengue per le persone che si sono infettate in luoghi in cui altri flavivirus potenzialmente cross-reattivi (come Zika, West Nile, febbre gialla e virus dell’encefalite giapponese) non sono presenti.
Nelle persone provenienti o residenti in aree dove sono presenti diversi flavivirus come Zika, West Nile, febbre gialla e virus dell’encefalite giapponese è probabile che i risultati siano falsificati per il fenomeno della cross-reattività. Per questo motivo devono essere eseguiti test diagnostici sia molecolari che sierologici per la dengue per identificare il virus, causa della malattia.
E’ possibile che persone vaccinate contro altri flavivirus (come la febbre gialla o l’encefalite giapponese) possono produrre anticorpi contro il flavivirus con reattività crociata, dando risultati falsi positivi ai test diagnostici, in particolare alla presenza di IgG.
Presso il Cesmet Clinica del viaggiatore sono disponibili i test diagnostici per la dengue (molecolari e sierologici). Per informazioni scrivi cliccando qui e lasciando i dati richiesti. Oppure telefona al numero +390639030481
Test diagnostici per dengue e campioni
| Test diagnostico | ≤ 7 giorni dopo l’esordio dei sintomi | >7 giorni dopo l’esordio dei sintomi | Tipi di campioni |
| Test Molecolari | ✓ | — | Siero, plasma, sangue intero, liquido cerebrospinale* |
| Rilevamento dell’antigene del virus dengue (NS1) | ✓ | — | Siero |
| Test sierologici | ✓ | ✓ | Siero, liquido cerebrospinale* |
| Test sui tessuti | ✓ | ✓ | Tessuto fisso |
* Il test del liquido cerebrospinale è raccomandato nei pazienti sospetti con manifestazioni cliniche del sistema nervoso centrale come encefalopatia e meningite asettica.
La fase acuta della malattia da virus dengue si sviluppa nei primi 1-7 giorni dopo l’esordio dei sintomi.
Durante questo periodo, il virus della dengue è presente nel sangue o nei fluidi derivati dal sangue come siero o plasma. L’RNA virale della dengue può essere rilevato con test molecolari. La proteina non strutturale NS1 è una proteina del virus della dengue che può essere rilevata con i test immunocromatografici e in immunofluorescenza.
Un risultato negativo di un test molecolare o NS1 non è definitivo nella diagnosi del virus. Per i pazienti sintomatici durante i primi 1-7 giorni di malattia, qualsiasi campione di siero deve essere testato mediante un test RT-PCR o NS1 e un test degli anticorpi IgM. L’esecuzione di test per anticorpi molecolari e IgM (o anticorpi NS1 e IgM) può rilevare più casi rispetto all’esecuzione di un solo test durante questo periodo di tempo e di solito consente la diagnosi con un singolo campione.
Il periodo oltre i 7 giorni dopo l’insorgenza dei sintomi è indicato come la fase di convalescenza della dengue. I pazienti con risultati negativi del test PCR o NS1 e test anticorpali IgM negativi dai primi 7 giorni di malattia devono sottoporsi a un test convalescente per il test degli anticorpi IgM.
Durante la fase di convalescenza, gli anticorpi IgM sono solitamente presenti e possono essere rilevati in modo affidabile da un test degli anticorpi IgM. Gli anticorpi IgM contro il virus della dengue possono rimanere rilevabili per 3 mesi o più dopo l’infezione.
I pazienti che hanno anticorpi IgM contro il virus della dengue rilevati nel loro campione di siero con un test per gli anticorpi IgM e che: 1) hanno un risultato NAAT o NS1 negativo nel campione della fase acuta, o 2) senza un campione della fase acuta, sono classificati come aventi un presunta, recente infezione da virus dengue.
Considerazioni speciali:
Non c’è un trattamento specifico per la febbre da Dengue. Solo una terapia sintomatica e una sorveglianza medica attenta può risolvere i problemi e salvare la vita a molti pazienti.
La terapia della “febbre da dengue”:
La terapia di supporto prevede l’utilizzo di farmaci antifebbrili, quale il paracetamolo e antidolorifici, scelti tra i FANS privi di proprietà anticoagulanti. Assolutamente da evitare l’aspirina (acido acetilsalicilico) e tutti i farmaci contenenti acetilati a causa delle loro proprietà anticoagulanti
I pazienti infettati dal virus, febbrili nella fase acuta, dovrebbero adottare criteri preventivi per evitare le punture di zanzare Aedes, che con questo pasto ematico si infettano ed amplificano ad altri individui, l’infezione.
La Febbre da virus Dengue durante la gravidanza
I dati della bibliografia tengono conto degli esiti sanitari della dengue in gravidanza e degli effetti dell’infezione materna sul feto nei mesi di gestazioni.
 I neonati con infezione perinatale in genere si ammalano durante la prima settimana di vita.
I neonati con infezione perinatale in genere si ammalano durante la prima settimana di vita.
 Prevenzione della febbre da virus della Dengue. Un modo efficace, ad oggi, per controllare la Dengue e la DHF è la lotta al vettore, ed in particolare combattere la presenza della zanzara Aedes nell’ambiente cittadino e silvestre.
Prevenzione della febbre da virus della Dengue. Un modo efficace, ad oggi, per controllare la Dengue e la DHF è la lotta al vettore, ed in particolare combattere la presenza della zanzara Aedes nell’ambiente cittadino e silvestre.Questo controllo avviene attraverso l’utilizzo di insetticidi chimici ambientali; e ancora ripulendo gli ambienti dove il vettore vive e si moltiplica sensibilizzando anche la popolazione che vive nei territori coinvolti. Attenzione particolare va posta alle raccolte di acqua, in particolare nelle gomme di automobili, bottiglie, lattine e altri oggetti luogo di ristagno di acqua, rendendo l’ambiente favorevole alla deposizione e schiusa delle uova di zanzara. Le larve sono trattate mediante l’utilizzo di insetticidi.
Ci sono state nel recente passato molte campagne in questo senso che hanno sensibilizzato la popolazione a ripulire l’ambiente circostante e le proprie case da gomme di automobili, bottiglie, lattine e altri oggetti nei quali l’acqua può ristagnare formando un habitat adatto per la zanzara. Le larve derivate dalla schiusa delle uova deposte dalle femmine di Aedes sono trattate mediante l’utilizzo di insetticidi. Dato che le zanzare sono più attive nelle prime ore del mattino, è particolarmente importante utilizzare le protezioni in questa parte della giornata.
la zanzara. Le larve derivate dalla schiusa delle uova deposte dalle femmine di Aedes sono trattate mediante l’utilizzo di insetticidi. Dato che le zanzare sono più attive nelle prime ore del mattino, è particolarmente importante utilizzare le protezioni in questa parte della giornata.
UTILIZZO DI REPELLENTI CONTRO LE ZANZARE AD USO PERSONALE.

Zanzare: come e di cosa si cibano
Le zanzare Aedes non si nutrono solo di sangue. Le femmine lo utilizzano, pungendo i mammiferi, quando hanno bisogno di energie per produrre le uova. Altre forme di nutrimento sono il nettare e la linfa che trovano nelle piante. Dopo la puntura compare un prurito molto fastidioso che è causato dalla saliva che la zanzara inietta nella pelle per evitare che il sangue coaguli e che la microscopica ferita cicatrizzi impedendole di succhiare la sua piccola dose di sangue.
REPELLENTI NATURALI
OLIO NOZETA: ESTRATTO DI NEEM con aggiunta di ESSENZE AROMATICHE POTENZIANTI
Un prodotto considerato tra i “migliori REPELLENTI” naturali. Multiuso, sicuro, efficace, estratto dal frutto dell’albero di NEEM, utilizzabile anche sui neonati, nei bambini e in coloro che desiderano evitare prodotti chimici, ha mostrato grande efficacia come repellente dalle punture degli insetti in generale, ed in modo particolare nei confronti delle punture delle zanzare. Questo prodotto è efficace anche nei confronti delle zecche.
efficace anche nei confronti delle zecche.
Nella formulazione per i viaggiatori questo olio, con l’aggiunta di “essenze” quali Corymbia citrodora, che ne potenzia l’efficacia e che ne migliora la fragranza e l’odore, possiede un utilizzo “multiplo”, nei confronti di parassiti e microbi, ed anche nelle ustioni.
CLICCA QUI PER APPROFONDIRE e CLICCA QUI PER ACQUISTARE
REPELLENTI CHIMICI
DEET dietiltoluamide: lo spray DEET costituisce un metodo efficace per tenere le zanzare lontane applicando un repellente sulla pelle e anche sui vestiti. La dietiltoluamide (DEET), è una sostanza chimica sviluppata dall’esercito statunitense durante la Seconda guerra mondiale e derivata dall’agricoltura, usata per tenere lontani i parassiti. Non va confusa con il DDT.
La DEET ha il problema che viene assorbita dalla pelle causando alla lunga problemi cutanei. Quindi in elevate concentrazioni non è raccomandata per i bambini (e in particolare non va mai usata sui bambini minori di due anni), e con pelli delicate. Consigliamo i repellenti Naturali a base di NEEM con aggiunta di essenze orientali.
ICARIDINA: L’icaridina (anche chiamata KBR 3023 o picaridina) è un prodotto sintetico sviluppato negli anni Ottanta e commercializzato dalle stesse aziende che vendono gli spray DEET. Alle giuste concentrazioni è efficace quanto la DEET, ma siccome rimane quasi completamente sulla pelle senza essere assorbita è più indicata anche per i bambini tra i due e i dodici anni.
Il primo vaccino per la dengue è stato realizzato già da diversi anni per i residenti nelle aree di rischio DENGUE e per i viaggiatori, tra i9 ed i 45 anni anni, che già avevano avuto la malattia in modo dimostrabile, attraverso la presenza di anticorpi IgG, ancora presenti: DENGVAXIA è il primo vaccino in commercio da diversi anni e approvato da FDA (americano) ed EMA (Europea). Utilizzato per la protezione delle popolazioni che vivono in paesi considerati ad alto rischio Dengue di età compresa tra i 9 ed i 45 anni di età.
Dal Dicembre 2022 in Europa Ema, ed in seguito dal febbraio 2023 in Italia è stato approvato il nuovo vaccino QDENGA della azienda TAKEDA. Questo nuovo vaccino è destinato alla popolazione, dai 4 anni in avanti sia che non ha avuto la malattia, sia da proteggere dagli aggravamenti nelle infezioni secondarie.
PER INFORMAZIONI SUL NUOVO VACCINO QDENGA CLICCA QUI
– TAK-003: vaccino ancora in via di studio, ma in dirittura d’arrivo. Attualmente in Fase 3.

Si sta cercando di ottenere una zanzara del genere Aedes modificata, in grado di essere resistente all’infezione virale in questione. Gli scienziati dell’Università della California di Irvine e i colleghi britannici di Oxford hanno messo a punto un nuovo ceppo di zanzare, in cui le femmine non possono volare, finendo così con il morire rapidamente allo stato selvatico. I maschi del ceppo possono volare, ma non mordono, dunque non trasmettono le malattie.
Quando le zanzare geneticamente modificate di sesso maschile si accoppiano con le femmine selvatiche e trasmettono i loro geni, le femmine della prossima generazione non saranno in grado di volare. Gli scienziati stimano che, se rilasciata la nuova razza potrebbe reprimere la popolazione della zanzara in sei – nove mesi. Inoltre, questo approccio potrebbe essere adattato anche per altre specie di zanzare, come Anopheles ossia quelle che propagano malattie come la malaria e “Culex“ Encefalite Giapponese.
Anche l’Italia farà parte del progetto di sperimentazione durante il prossimo inverno. Si stanno facendo degli studi sulla patogenesi nell’infezione da Dengue dell’ospite, facendo degli studi anche sulla storia dell’individuo e la delineazione dei caratteri dei gruppi più ad alto rischio. Ancora si stanno facendo ricerche sulle dinamiche di trasmissione e sulla genetica delle popolazioni colpite.
Scheda malattia Dengue Leggi tutto »
La Cina, con la sua vasta estensione geografica e diversità climatica, presenta un complesso quadro epidemiologico di malattie infettive che varia considerevolmente tra le diverse regioni e nel cambiamento delle stagioni.
Negli ultimi decenni, la Cina ha registrato un notevole decremento dell’incidenza e della mortalità per malattie infettive, passando da circa 4000 casi ogni 100.000 abitanti nel 1970 a circa sotto i 2oo casi per 100.000 nel 20017. Nonostante questi progressi le malattie storicamente endemiche persistono in determinate aree e nuove minacce epidemiche che emergono periodicamente.
Le cinque malattie infettive più frequenti nel paese sono
la tubercolosi,
l’epatite B,
la dissenteria, diarrea da agenti intestinali aggressivi,
la sifilide
la gonorrea.
Negli ultimi cinque anni si è osservato un incremento delle malattie a trasmissione sessuale.
La tubercolosi resta una delle principali cause di morbilità, con la Cina che rappresentava l’8,5% dei nuovi casi globali nel 2020, classificandosi come il terzo paese al mondo per incidenza di tubercolosi dopo India e Indonesia.
Dopo l’esperienza della SARS nel 2003, il governo cinese ha implementato un sistema di risposta alle emergenze sanitarie più coordinato, con meccanismi per il rilevamento precoce dei focolai e una migliore comunicazione tra i diversi livelli di governo. Questo sistema è stato ulteriormente messo alla prova e rafforzato durante la pandemia di COVID-19.
VIAGGIARE IN CINA tra gli animali:
una analisi approfondita del “Rischio Rabbia” e Indicazioni per viaggiare in Cina in sicurezza.
La Rabbia in Cina, una analisi epidemiologica
Contesto Storico e Situazione Attuale: Il successo del controllo della Rabbia nel paese diventa un paradosso
La Repubblica Popolare Cinese ha una lunga storia nella lotta contro la rabbia, una malattia degli animali, di origine virale, con un tasso di letalità prossimo al 100% una volta che si manifestano i sintomi clinici.
dagli anni ’50 la Cina ha affrontato tre ondate epidemiche principali:
(1) nel 1956 furono registrati 1.942 casi;
(2) nel 1981 i casi furono 7.037;
(3) nel 2007 3.300 furono i casi documentati.
Questi dati evidenziano la natura endemica e persistente ……….
MALATTIE TRASMESSE DA VETTORI
Malaria
Storicamente, la malaria è stata una delle principali malattie endemiche in Cina, con focus nelle zone rurali di diverse province. Il rischio di infezione malarica era presente nelle zone rurali delle province di Anhui, Guizhou, Hainan, Henan, Hubei e Yunnan. Plasmodium vivax e Plasmodium falciparum sono state le due specie di malaria principali, con la malaria da P. vivax che rappresentava il 95% dei casi indigeni, mentre l’endemia da P. falciparum era limitata alle province di Yunnan e Hainan.
È importante notare che la Cina ha ricevuto la certificazione “Malaria free” dall’OMS nel 2021, dopo che in precedenza si registravano rari casi nelle contee lungo il confine con la Birmania nella provincia di Yunnan e nella contea di Motuo in Tibet. Questo rappresenta un importante traguardo per la salute pubblica cinese.
Dengue
Focolai di febbre dengue sempre maggiori si verificano periodicamente in Cina, in molte provincie ma principalmente nelle province meridionali di Guangdong, Guangxi, Hainan e Yunnan.
La dengue è oramai considerata endemica dal 2023, e le epidemie stagionali sono un problema ricorrente, soprattutto con l’aumento delle temperature globali che favorisce l’espansione dell’habitat delle zanzare vettori.
I dati mostrano una chiara stagionalità, con il 61,9% dei casi importati che si verificano tra luglio e ottobre, e indici stagionali particolarmente elevati in agosto (2,23) e ottobre (2,38). Questa distribuzione temporale corrisponde alle stagioni di maggiore attività del vettore nelle regioni tropicali e subtropicali.
Chikungunya
Focolai epidemici di chikungunya sono sporadici e segnalati principalmente dalla provincia di Guangdong. Questa malattia, anch’essa trasmessa da zanzare, mostra un pattern simile alla dengue in termini di distribuzione geografica, essendo più prevalente nelle province meridionali con clima favorevole alla riproduzione delle zanzare Aedes.
Encefalite Giapponese
L’encefalite giapponese rappresenta un problema sanitario significativo in alcune aree della Cina. I casi si verificano con regolarità nelle aree rurali, in particolare nelle province di Henan, Shaanxi e Shanxi (Yuncheng City). Il rischio è diffuso in tutte le province tranne le aree nord-orientali di Xinjiang e Qinghai.
La trasmissione dell’encefalite giapponese mostra un chiaro pattern stagionale, con la maggior parte dei casi segnalati da giugno a ottobre. Questo coincide con i cicli di vita del vettore (zanzare Culex) e la presenza degli ospiti amplificatori come maiali e uccelli acquatici.
Leishmaniosi
La Cina registra casi sporadici di leishmaniosi, con distribuzione geografica variabile. Casi di leishmaniosi viscerale si verificano nella provincia di Xinjiang, nella parte occidentale della Mongolia interna e nella provincia di Fujian (nella parte sud-orientale della Cina). I casi di leishmaniosi cutanea sono stati riportati principalmente dalla provincia di Xinjiang.
MALATTIE ENDEMICHE A TRASMISSIONE DIRETTA
Tubercolosi
La tubercolosi rappresenta una delle principali sfide sanitarie in Cina. Nel 2020, la Cina ha registrato l’8,5% dei nuovi casi di tubercolosi a livello mondiale, classificandosi al terzo posto dopo India e Indonesia
La diffusione della tubercolosi è relativamente uniforme in tutto il territorio cinese, sebbene le aree rurali e le regioni con minore accesso ai servizi sanitari tendano ad avere tassi più elevati.
La tubercolosi in Cina è strettamente correlata a fattori socioeconomici, con una maggiore prevalenza nelle aree meno sviluppate. Il trattamento standard in Cina prevede due fasi di terapia:
una fase intensiva con quattro antibiotici per 2 mesi,
seguita da una fase di continuazione con solo due antibiotici per 4-7 mesi.
Epatite virale B – A
L’epatite B è endemica in Cina ed è una delle cinque malattie infettive più frequenti nel paese. La prevalenza dell’epatite B è diminuita significativamente grazie ai programmi di vaccinazione, ma rimane un importante problema di salute pubblica, soprattutto nelle aree rurali e nelle regioni occidentali meno sviluppate.
L’epatite A e l’epatite E sono anch’esse presenti, con focolai occasionali legati a contaminazione dell’acqua o degli alimenti. L’epatite E in particolare è stata segnalata come malattia presente in Cina.
Brucellosi
La brucellosi umana è diffusa nelle aree rurali della Cina. Un aumento del numero di casi è stato segnalato nel giugno 2012 tra i lavoratori del latte della provincia di Heilongjiang, nel nord-est del paese1. La prevalenza più alta di brucellosi umana si osserva nelle province centro-orientali di Shanxi, Hebei e Henan.
Questa zoonosi è strettamente legata all’allevamento di animali, in particolare bovini, ovini e caprini, e rappresenta un rischio occupazionale per allevatori e lavoratori dell’industria lattiero-casearia. La distribuzione geografica riflette le aree con maggiore concentrazione di allevamenti.
MALATTIE TRASMESSE DALL’ACQUA E DAL CIBO
Schistosomiasi
La Cina presenta un elevato rischio di parassitosi intestinale da Schistosoma japonicum. Un focus endemico di schistosomiasi è costituito dal bacino idrografico del fiume Azzurro (Yangtze), dove le condizioni ambientali favoriscono il ciclo di vita del parassita.
I programmi di controllo hanno ridotto significativamente la prevalenza della schistosomiasi nelle ultime decadi, ma la malattia persiste in alcune aree, rappresentando un esempio di malattia tropicale negletta in Cina.
Colera
Focolai di colera sono segnalati sporadicamente in Cina. I più recenti sono stati riportati dal paese di Mengcheng nella parte orientale della provincia di Anhui e da una scuola nella città di Huaian nella provincia di Jiangsu. Nei sobborghi delle grandi città di shanghai e Pechino. Il colera tende a manifestarsi in situazioni di carenza igienico-sanitaria, particolarmente dopo disastri naturali o in aree con infrastrutture idriche inadeguate.
MALATTIE EPIDEMICHE E FOCOLAI RECENTI
Coronavirus e Pandemie
COVID-19
La pandemia di COVID-19, originata a Wuhan, nella provincia di Hubei, a fine 2019, ha rappresentato la crisi sanitaria più significativa degli ultimi anni in Cina e nel mondo. Il primo paziente confermato ha iniziato a manifestare sintomi già il 1º dicembre 2019. Al 6 gennaio 2023, la Cina aveva registrato 471.373 casi confermati, con 373.256 guariti e 5.264 morti. La pandemia è stata dichiarata conclusa dall’OMS il 5 maggio 2023.
La risposta della Cina alla pandemia ha incluso misure drastiche come il blocco di Wuhan e dell’intera provincia di Hubei, l’interruzione dei trasporti e la costruzione rapida di ospedali dedicati. La strategia “zero COVID” adottata dal paese ha comportato limitazioni ai viaggi, test di massa e quarantene rigorose per contenere i focolai.
Recentemente, si è ipotizzata una nuova ondata di COVID con picco previsto per fine giugno di circa 65 milioni di casi a settimana, secondo il prof. Zhong Nanshan, esperto di malattie respiratorie in Cina. La variante Xbb di Omicron sarebbe la causa di questo aumento, con un tasso di infezione passato dallo 0,2% di metà febbraio al 74,4% di fine aprile e all’83,6% di inizio maggio 2022.
SARS
L’epidemia di SARS (Sindrome Respiratoria Acuta Grave) del 2003 ha colpito duramente la Cina, che ha riportato il 66% dei casi e il 45% delle morti a livello mondiale. Questa esperienza ha portato a significativi cambiamenti nel sistema di risposta alle emergenze sanitarie del paese, inclusa l’implementazione di un sistema di sorveglianza più robusto.
La SARS e le altre zoonosi, che rappresentano le principali malattie infettive emergenti, sono state ricondotte alle condizioni di promiscuità fra persone ed animali domestici, caratteristiche della cultura cinese. Questa esperienza ha influenzato l’approccio alla successiva pandemia di COVID-19.
Malattie Respiratorie Emergenti
Metapneumovirus Umano (HMPV)
Recentemente, è stato registrato un aumento dei casi di metapneumovirus umano (HMPV) in Cina e in altri paesi asiatici.
Alla fine del 2024, in Cina questo virus è stato collegato al 6,2% dei test positivi per le malattie respiratorie e al 5,4% dei ricoveri ospedalieri, più del COVID-19, del rinovirus o dell’adenovirus.
I casi sono in aumento principalmente nel nord della Cina, soprattutto tra i bambini sotto i 14 anni. Secondo le autorità sanitarie cinesi, il tasso di casi positivi nelle province settentrionali è in calo, anche se i dati sono fluttuanti. Questo virus, che appartiene alla stessa famiglia del virus respiratorio sinciziale, provoca nella maggioranza dei casi sintomi influenzali o simili al raffreddore.
Polmonite nei Bambini
Da metà ottobre 2024, la Cina settentrionale ha registrato un aumento delle malattie simil-influenzali rispetto allo stesso periodo dei tre anni precedenti. Il 21 novembre 2024 sono stati segnalati cluster di polmonite non diagnosticata nei bambini nel nord della Cina.
Le autorità cinesi hanno attribuito l’aumento alla revoca delle restrizioni anti-Covid e alla circolazione di agenti patogeni come l’influenza, il micoplasma pneumoniae, il virus respiratorio sinciziale (RSV) e il SARS-CoV-2. Secondo l’Organizzazione Mondiale della Sanità, i livelli di infezioni respiratorie segnalati in Cina rientrano nei normali intervalli della stagione invernale.
DISTRIBUZIONE REGIONALE DELLE MALATTIE INFETTIVE
Regioni Settentrionali
Le regioni settentrionali della Cina presentano un profilo epidemiologico caratterizzato principalmente da malattie respiratorie, specialmente durante i mesi invernali. Recentemente si è osservato un aumento di casi di metapneumovirus umano e altre infezioni respiratorie in queste aree.
La brucellosi è particolarmente presente nelle aree rurali delle province settentrionali, con un’alta prevalenza nella provincia di Heilongjiang. Anche l’antrace è stato segnalato nelle province di Liaoning e Jiangsu.
Regioni Centrali
Nelle province centrali come Henan, Shaanxi e Shanxi, l’encefalite giapponese si verifica con regolarità nelle aree rurali. La brucellosi mostra un’alta prevalenza nelle province centro-orientali di Shanxi, Hebei e Henan.
La schistosomiasi è endemica nel bacino del fiume Yangtze, che attraversa diverse province centrali1. Questa malattia è strettamente legata alle pratiche agricole e alla presenza di molluschi d’acqua dolce che fungono da ospiti intermedi.
Regioni Meridionali
Le province meridionali di Guangdong, Guangxi, Hainan e Yunnan rappresentano l’area principale per le malattie trasmesse da vettori come dengue e chikungunya. Queste regioni hanno un clima tropicale o subtropicale che favorisce la proliferazione delle zanzare vettori.
La provincia di Yunnan, al confine con il Myanmar, ha storicamente registrato casi di malaria, principalmente nelle aree rurali. Anche Hainan, un’isola tropicale, è stata una delle due province con endemia da P. falciparum.
La rabbia è particolarmente diffusa nella regione autonoma Zhuang del Guangxi e nelle province meridionali di Guizhou, Guangdong, Hunan e Sichuan1.
Regioni Occidentali
Nella provincia di Xinjiang, nella parte occidentale della Cina, si verificano casi di leishmaniosi sia viscerale che cutanea. Questa regione, caratterizzata da un ambiente desertico e semi-desertico, presenta condizioni ecologiche favorevoli alla presenza dei vettori della leishmaniosi.
Il rischio di encefalite giapponese è minore nelle aree nord-orientali di Xinjiang e Qinghai rispetto al resto del paese, probabilmente a causa delle condizioni climatiche meno favorevoli alla riproduzione delle zanzare vettori.
Modelli Stagionali delle Malattie Infettive
Malattie Respiratorie (Stagione Invernale)
Le infezioni respiratorie mostrano un chiaro pattern stagionale in Cina, con aumenti significativi durante i mesi invernali, particolarmente nelle regioni settentrionali del paese. Da metà ottobre, la Cina settentrionale ha registrato un aumento delle malattie simil-influenzali rispetto allo stesso periodo dei tre anni precedenti.
L’influenza rappresenta il principale agente patogeno respiratorio in inverno, con oltre il 30% dei test positivi e il 17% dei ricoveri ospedalieri9. Altri agenti patogeni respiratori significativi durante l’inverno includono il virus respiratorio sinciziale (RSV), il metapneumovirus umano (HMPV) e il Mycoplasma pneumoniae9.
È importante notare che gli aumenti stagionali delle infezioni respiratorie nei paesi dell’emisfero settentrionale, inclusa la Cina, rientrano nei normali intervalli per la stagione invernale.
Malattie Trasmesse da Vettori (Stagione Estiva-Autunnale)
Le malattie trasmesse da vettori mostrano un chiaro pattern stagionale in Cina, con picchi durante i mesi caldi quando le zanzare e altri vettori sono più attivi.
Dengue
La dengue mostra una marcata stagionalità, con il 61,9% dei casi importati che si verificano tra luglio e ottobre. L’indice stagionale è particolarmente alto in agosto (2,23) e ottobre (2,38). Questa distribuzione temporale corrisponde alle stagioni di maggiore attività delle zanzare Aedes.
Encefalite Giapponese
La maggior parte dei casi di encefalite giapponese sono segnalati da giugno a ottobre7, periodo che coincide con la maggiore attività delle zanzare Culex e con la presenza degli ospiti amplificatori come maiali e uccelli acquatici.
Malaria
Sebbene la Cina sia ora certificata come “Malaria free”, i casi importati mostrano alcune variazioni stagionali. I numeri di casi di P. falciparum erano più alti in maggio (86 casi) e luglio (83 casi), mentre i casi di P. vivax si verificavano più frequentemente in maggio (23 casi) e agosto (23 casi). Tuttavia, le caratteristiche stagionali dei casi importati di malaria non erano particolarmente evidenti dal 2011 al 20164, con un’incidenza generalmente bassa in febbraio, marzo, novembre e dicembre4.
Misure d Protezione Individuale
Per i viaggiatori e i residenti in aree a rischio di malattie trasmesse da vettori, si raccomandano diverse misure di protezione individuale:
1. Evitare di soggiornare all’aperto nelle ore in cui i vettori sono attivi
2. Indossare abiti di colore chiaro con maniche lunghe e pantaloni lunghi
3. Utilizzare repellenti per insetti naturali a basee di olio di Neem oppure contenenti DEET, IR3535 o Icaridina
4. Soggiornare in stanze dotate di condizionatore d’aria o zanzariere a porte e finestre
5. Utilizzare zanzariere da letto, rimboccandone i margini sotto il materasso
Queste misure, se correttamente implementate, possono ridurre del 90% il rischio di contrarre malattie come la malaria
Cina – 05 – Quali sono le malattie presenti nel paese? Quali sono i rischi reali? Leggi tutto »
La situazione della Chikungunya in Italia nel 2025 è sotto controllo, ma monitorata con attenzione dalle autorità sanitarie. I dati aggiornati al 12 agosto 2025 indicano quanto segue:
• Sono stati registrati 43 casi confermati di Chikungunya dall’inizio dell’anno.
– 36 casi sono importati (persone tornate da viaggi in aree endemiche).
– 7 casi sono autoctoni (ossia con trasmissione avvenuta in Italia).
• La maggior parte dei casi si concentra nel nord e nel centro Italia, ma si sono verificati episodi autoctoni in alcune Regioni, in particolare Emilia-Romagna.epicentro.iss+2
• Non sono stati riportati decessi associati.
• L’età mediana dei casi è di 48 anni, con una lieve prevalenza nel sesso maschile.
Le autorità sanitarie, tra cui l’Istituto Superiore di Sanità e il Ministero della Salute, continuano a monitorare la diffusione tramite bollettini e piani di sorveglianza specifici.
Considerazioni generali:
• La Chikungunya in Italia non è considerata endemica: alcuni focolai autoctoni si verificano grazie alla presenza della zanzara Aedes albopictus (“zanzara tigre”), ma la larga maggioranza dei casi è legata a viaggi all’estero
• A livello europeo sono previsti possibili aumenti di casi, in relazione al clima e alle nuove dinamiche di viaggio.
• I sintomi più comuni restano febbre alta e forti dolori articolari, con un decorso generalmente benigno.
Non è motivo di allarme, ma è importante adottare precauzioni contro le punture di zanzara durante la stagione estiva e se si viaggia in zone dove il virus è endemico
La mappa (da ECDC) mostra anche le localizzazioni dei casi autoctoni in Francia, dove il totale dall’inizio dell’anno arriva a 111 casi.
Nella tabella che segue (da ECDC) i dettagli relativi ai casi in Italia
Casi autoctoni di Chikungunya in Europa Leggi tutto »
Introduzione al Virus West Nile (WNV)
Cenni Storici e Diffusione Globale
Il Virus West Nile (WNV) fu isolato per la prima volta nel 1937, casualmente, da una donna con febbre elevata, dolori, problemi oftalmici avanzati, nel distretto del West Nile in Uganda.
questa arbovirosi rappresenta oramai in tutto il mondo un reale problema di salute pubblica, coinvolgendo animali ed umani. Dalla presenza in alcune aree forestali ugandesi e della fasciatropicale e del Medio Oriente, è diventato causa di epidemie in equini e nell’uomo in tutto il mondo. Dagli anni ’90, WNV ha diffuso senza precedenti con una patologia neuro-invasiva nell’uomo e negli equidi (cavalli e muli) in Europa. In Romania nel 1996 un importante focolaio e successivamente a New York nel 1999 con un gravissimo focolaio. In seguito si è diffuso in tutto il continente americano e poi nell’emisfero nord.
Fin dal 1950 in Egitto e dal 1951 in Israele si è diffuso nel bacino del mediterraneo, con i primi i primi casi in Europa meridionale nel 1962 in Francia. Da allora il virus è comparso anche in Italia, in particolare nelle campagne Toscane, coinvolgendo soprattutto cavalli degli allevamenti locali. Questa diffusione costante, soprattutto nelle regioni temperate del Nord America e dell’Europa, legata alla migrazione degli uccelli selvatici da passo, ha caratterizzato il WNV come un patogeno emergente e riemergente, la cui trasmissione è strettamente legata a fattori ecologici, climatici e umani.
Il Virus: Classificazione e Lignaggi Genetici
West Nile Virus è un virus a RNA a singolo filamento positivo, del genere dei Flavivirus. È un arbovirus collegato e appartenente alla famiglie a cui afferisce anche l’encefalite giapponese ed altri importanti virus neurotropi.
Il suo genoma codifica per una “poliproteina”, proteina multipla, che viene successivamente suddivisa e scissa in tre proteine strutturali: (1) il capside (C); (2) la pre-membrana (prM); (3) l’involucro (E); insieme a queste 3 proteine principali vengono prodotte sette proteine non strutturali (NS1, NS2A, NS2B, NS3, NS4A, NS4B, NS5). La proteina di involucro (E) è quella “chiave” che media l’attacco del virus al recettore delle cellule ospiti. Questa proteina di attacco è il principale bersaglio degli anticorpi neutralizzanti. E’ questa la proteina chiave su cui si stanno studianodo i nuovo vaccini.
L’analisi filogenetica ha consentito la classificazione del WNV in almeno otto lignaggi genetici. Tuttavia, dal punto di vista epidemiologico e clinico, i lignaggi 1 (L1) e 2 (L2) sono considerati i puù importanti ma anche i più aggressivi per l’uomo e gli animali.
Il lignaggio 1 ha causato i grandi focolai epidemici in Europa, nel Mediterraneo ma anche nelle Americhe.
Il lignaggio 2, da sempre diffuso in Africa sub-sahariana è considerato meno virulento, ed è comparso in Europa nel 2004 in Ungheria diffondendo poi in Grecia, Italia e altri paesi dell’Europa centrale e orientale, con un potenziale patogeno paragonabile a quello del lignaggio 1.
Attualmente i due lignaggi circolano contemporaneamente e caratterizzano un aspetto cruciale dell’attuale epidemiologia del WNV in Europa.
Il Ciclo di Trasmissione: Vettori, Serbatoi e Ospiti Accidentali
Il WNV sopravvive, si moltiplica e diffonde in natura attraverso un ciclo che coinvolge zanzare e uccelli. Gli uccelli, in particolare quelli appartenenti all’ordine dei Passeriformi (corvidi e passeri), sono ospiti serbatoio e amplificano il virus al loro interno tanto da sviluppare una elevata viremia sufficiente ad infettare le zanzare che pungono per cibarsi del loro sangue. In questo modo, da un uccello e l’altro, con punture infette ricche di virus si perpetua il ciclo vitale e la moltiplicazione.
I vettori del WNV sono le zanzare del genere Culex. La specie Culex pipiens è diffusa in Europa e in Italia. Queste zanzare si nutrono con sangue di uccelli pungono occasionalmente anche i mammiferi, fungendo da “vettori ponte” e causando la trasmissione del virus a ospiti accidentali e afondo cieco, cioè non capaci di trasmettere ulteriormente il virus.
Difatti l’uomo e i cavalli ed asini sono considerati ospiti non “trasmettitori”. Difatti sviluppano una malattia, talvolta in forma grave, ma la loro viremia è troppo bassa da poter infettare una zanzara che punge l’uomo o gli equini, rendendoli praticamente incapaci di trasmettere il virus e di contribuire al suo ciclo naturale. Con questa caratteristica è possibile realizzare un controllo epidemiologico adeguato e strategie di interruzione della catena di trasmissione della malattia. Alcune recenti ricerche hanno evidenziato che in determinate circostanze, per fortuna rare, la trasmissione del virus da mammifero a zanzara può avvenire Ciò può avere implicazioni significative per la valutazione del rischio di diffusione della malattia.
Altre vie di infezione alternative nell’uomo, piuttosto rare includono le “trasfusioni di sangue” e di “emocomponenti”, i “trapianti di organi solidi” e di “cellule staminali emopoietiche”.
Il virus può essere trasmesso anche “verticalmente” dalla madre al feto durante la gravidanza e, in via teorica” attraverso l’allattamento al seno.
Queste vie alternative sono di molto importanti per seguire lo sviluppo di una epidemia ed ancora per impostare regole di contenimento della epidemia stessa.
Nell’uomo, dopo la puntura dell’insetto vettore, il virus si replica nelle cellule di Langerhans del derma, che migrano verso la rete linfatica e, quindi, verso il torrente circolatorio. Questa fase corrisponde alla prima viremia, durante la quale il virus si diffonde in tutti gli organi del sistema linfatico. Successivamente avviene una seconda gittata viremica che corrisponde alla seconda viremia. Il virus può essere isolato nel sangue dopo 1-2 giorni dalla puntura dell’insetto vettore fino a poco più di una settimana. La comparsa nel siero di anticorpi di tipo IgM coincide con il termine della viremia. La viremia da West Nile Virus è a basso titolo nell’uomo ed è assente al momento della comparsa dei sintomi.
. In questo gruppo sono compresi anche i virus responsabili dell’Encefalite di St. Louis, Encefalite della Valle del Murray, il virus Usutu, Kunjin, Kokobera, Stratford e Alfuy.

La Cute, tramite puntura della zanzara vettore durante il pasto ematico.
Il virus West Nile è trasmesso sia negli animali che all’uomo tramite la puntura di zanzare infette. Altri mezzi di infezione documentati, anche se molto più rari, sono trapianti di organi, trasfusioni di sangue e la trasmissione madre-feto in gravidanza. Il virus infetta diversi mammiferi, soprattutto equini, ma in alcuni casi anche cani, gatti, conigli e altri. E’ importante sottolineare che il virus non si trasmette da persona a persona, né da cavallo a persona attraverso la puntura di una zanzara infetta a causa dei bassi livelli di viremia.
Il periodo di incubazione dal momento della puntura della zanzara infetta varia fra 2 e 14 giorni, ma può essere anche di 21 giorni nei soggetti con deficit a carico del sistema immunitario.
Epidemiologia del Virus West Nile
Scenario Globale ed Europeo (Aggiornamento Agosto 2025)
Il Virus West Nile si è ormai diffuso nella maggior parte dei continenti ed in moltissimi paesi in tutto il mondo. In Africa, Medio Oriente, Asia, Nord America e in molti paesi del bacino del Mediterraneo ed anche dell’Europa continentale. In Europa le epidemie hanno un andamento stagionale, con la loro presenza evidente tra i mesi di giugno e di novembre, in coincidenza con i le condizioni del clima sempre più favorevoli. Caldo tropicale, umidità elevata,
L’Epidemia Italiana del 2025: Un’Analisi Approfondita
Dati Nazionali e Confronto con le Stagioni Precedenti (agosto 2025)
Il primo caso autoctono in Italia che ha aperto la stagione di trasmissione di WNV si è manifestato in Piemonte con un caso umano segnalato molto precocemente ossia il 20 marzo.
La situazione di WNV è rimasta silente durante i mesi di aprile -giugno per poi manifestarsi in tutta la sua gravità nel luglio 2025, dopo un giugno torrido, umido e favorevole alla crescita delle zanzare, in particolare della CULEX.
CLICCA QUI PER I DATI AGGIORNATI DI WEST NILE VIRUS IN ITALIA, IN EUROPA, NEL MONDO
La circolazione di WN in Europa e Meccanismi di “Overwintering”
La presenza annuale, oramai da quasi un decennio di casi umani e animali in paesi del Mediterraneo come l’Italia e la Grecia e nelle coste del Nord Africa conferma che WNV non è più presente sporadicamente ed importato dai paesi esotici, ma si è oramai stabilmente insediato ed è diventato endemico in molte regioni d’Europa. Quindi ci si chiede: come sopravvive il virus durante i mesi invernali, con temperature rigide; e possono le temperature introno allo zero interrompere l’attività delle zanzare?
Questo processo è chiamato “overwintering” ossia svernamento, superamento del periodo invernale; e questo diventa un fattore cruciale e determinante per comprendere la persistenza del virus nell’ambiente e prevedere l’inizio e l’intensità delle stagioni in cui i focolai epidemici ridiventeranno attivi.
I meccanismi proposti sono principalmente due:
(1) la persistenza nell’ambiente del virus, all’interno delle zanzare adulte che entrano in uno stato di dormienza invernale, la diapausa. Questo avviene in luoghi protetti come cantine, grotte, e ambienti umidi e riscaldati.
(2) la reintroduzione annuale del virus WN da parte degli “uccelli migratori” che rientrano dopo aver svernato in Africa.
Sono stati eseguiti in Nord America ed in Europa studi che hanno confermato che WNV può svernare nelle popolazioni di zanzare, consentendo una ripresa rapida della trasmissione al ripristino delle condizioni meteo favorevoli. D’altra parte altri studi in Francia non hanno confermato la presenza del virus nelle zanzare in pausa suggerendo che in quella specifica regione la reintroduzione tramite gli uccelli migratori rimanere il fattore predominante di reinfestazione.
A questa situazione ecologica si aggiunge la presenza evolutiva e geografica di vari lignaggi del virus a livello continentale. Storicamente, il lignaggio 1 del WNV è stato predominante in Europa occidentale, mentre il lignaggio 2 era presente e diffondeva nell’Europa orientale e all’Africa. Negli ultimi due decenni, si è assistito ad una espansione del lignaggio 2 verso l’ovest europeo, causando importanti epidemie in Grecia, Romania e Italia. Un evento epidemiologico di grande rilevanza si è verificato nel 2024, con la segnalazione del primo caso umano autoctono di malattia neuro-invasiva da WNV lignaggio 2 in Spagna.
Gli studi hanno evidenziato che i ceppi virali erano correlati a quelli circolanti in Europa centrale, e non a ceppi precedentemente isolati in Spagna. Questo caratterizza un salto geografico di questo tipo di virus verso ovest. Tutto questo evidenzia un panorama epidemiologico europeo in piena evoluzione.
La maggior parte delle persone infette non mostra alcun sintomo. Fra i casi sintomatici, circa il 20% dei soggetti sviluppa una malattia sistemica febbrile chiamata comunemente febbre di West Nile (WNF) caratterizzata dalla comparsa di febbre, cefalea, nausea, vomito, linfoadenopatia, possibili eruzioni cutanee. Generalmente questa fase acuta si risolve in una settimana o poco più, e possono variare molto a seconda dell’età della persona. Nei bambini è più frequente una febbre leggera, nei giovani la sintomatologia è caratterizzata da febbre mediamente alta, arrossamento degli occhi, mal di testa e dolori muscolari. Negli anziani e nelle persone debilitate, invece, la sintomatologia può essere più grave.
I sintomi più gravi si presentano in media in meno dell’1% delle persone infette (1 persona su 150), manifestandosi come una malattia neuro-invasiva (encefalite, meningo-encefalite, paralisi flaccida), con possibile decorso fatale. Il rischio di contrarre la forma neurologica della malattia aumenta all’aumentare dell’età ed è particolarmente elevato nei soggetti di età superiore ai 60 anni. Viceversa, in uno studio di sorveglianza effettutato negli Stati Uniti tra il 1998 e il 2008, è emerso che le paralisi flaccide acute sono state segnalate in percentuale maggiore in soggetti di età inferiore ai 60 anni. La letalità delle forme neuro-invasive si aggira intorno al 9% nei soggetti anziani e meno dell’1% nei bambini.
La diagnosi nell’uomo viene prevalentemente effettuata attraverso test di laboratorio (Elisa o Immunofluorescenza) effettuati su siero e, dove indicato, su fluido cerebrospinale, per la ricerca di anticorpi del tipo IgM. Questi anticorpi possono persistere per periodi anche molto lunghi nei soggetti malati (fino a un anno), pertanto la positività a questi test può indicare anche un’infezione pregressa. La siero-conversione o l’aumento di 4 volte del titolo anticorpale può essere utilizzata per diagnosticare un’infezione recente. I campioni raccolti entro 8 giorni dall’insorgenza dei sintomi potrebbero risultare negativi, pertanto è consigliabile ripetere a distanza di tempo il test di laboratorio prima di escludere la malattia. In alternativa la diagnosi può anche essere effettuata attraverso Pcr o coltura virale su campioni di siero e fluido cerebrospinale entro 7 giorni dall’inizio della sintomatologia acuta, tenendo conto che la viremia è relativamente di breve durata e di basso titolo.
Non esiste un vaccino per la febbre West Nile. Attualmente sono allo studio dei vaccini, ma per il momento la prevenzione consiste soprattutto nel ridurre l’esposizione alle punture di zanzare.
Pertanto è consigliabile proteggersi dalle punture ed evitare che le zanzare possano riprodursi facilmente:
· usando repellenti e indossando pantaloni lunghi e camicie a maniche lunghe quando si è all’aperto, soprattutto all’alba e al tramonto
· usando delle zanzariere alle finestre
· svuotando di frequente i vasi di fiori o altri contenitori (per esempio i secchi) con acqua stagnante
· cambiando spesso l’acqua nelle ciotole per gli animali.
Il controllo nei confronti della WND si basa essenzialmente sulla sorveglianza degli uccelli stanziali di specie sinantropiche, degli equidi e dell’avifauna selvatica di specie migratorie.
Non esiste una terapia specifica per la febbre West Nile, il trattamento è solo sintomatico. Nella maggior parte dei casi, i sintomi scompaiono da soli dopo qualche giorno o possono protrarsi per qualche settimana. Nei casi più gravi è invece necessario il ricovero in ospedale, dove i trattamenti somministrati comprendono fluidi intravenosi e respirazione assistita. Vi sono recentissime segnalazioni in letteratura che suggeriscono, su modelli animali, la possibile efficacia del trattamento con immunoglobuline specifiche anti WNV.
Febbre da West Nile Virus – Scheda malattia Leggi tutto »
Una mappa della situazione Dengue nei vari paesi del mondo (dati OMS) e la situazione degli ultimi mesi (ECDC).
Situazione mondiale Dengue Leggi tutto »